药品批准帮助年轻患者罕见癌症的斗争中

儿童和成年人与一种罕见的软组织癌症现在将有一个新的治疗选择有很大的影响。
美国食品和药物管理局批准免疫治疗药物atezolizumab (Tecentriq)患者使用先进的肺泡软肉瘤(asp)的一部分,已经扩散到身体的其他部位或无法切除的手术。
“这批准将产生巨大影响的一种罕见的疾病,尤其具有挑战性的治疗,”说爱丽丝博士陈发展治疗诊所的美国国家癌症研究所(NCI)的癌症治疗和诊断(DCTD)。
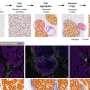
这种癌症开始连接和周围的软组织器官和其他组织。它慢慢扩散,但一旦传播通常是致命的。化疗不工作和新的靶向治疗,包括药物酪氨酸激酶抑制剂,没有持久的效果。
在美国大约有80人收到一个asp每年诊断。大约50%的转移性疾病患者还活着后五年。癌症主要影响青少年和年轻的成年人。
批准后被授予非随机性第二阶段的结果试验NCI为首的一部分,美国国家卫生研究院(NIH)。这种药物被批准人2岁以上。
试验中大约40%的患者治疗在马里兰州,美国国立卫生研究院临床中心说詹姆斯·朵罗修博士DCTD主任。
“我们能够把来自世界各地的病人是一个关键因素在做研究的能力,“朵罗修NCI说新闻发布会上。
这是第一个研究NCI-funded实验疗法临床试验网络,导致了药物的批准。
”这是一个重大的里程碑调查人员在实验疗法临床试验网络,以及asp病人社区,研究和罕见的癌症,”研究负责人说兰德博士沙龙。
这也标志着首次批准药物已经批准用于儿童。儿科肿瘤学部门在国家癌症研究中心的帮助招收儿童试验中,陈先生说。
“这项研究是一个重要的儿童之间的协作和医学肿瘤学的例子,让孩子非常罕见的癌症新疗法有效,”说约翰·Glod博士儿科肿瘤学的分支。“整个研究团队感谢患者参与了这项研究,使这项工作成为可能。”
Atezolizumab通过帮助工作免疫系统癌症的反应更强烈。检查点anti-PD-L1免疫抑制剂,药物被批准一些癌症患者,包括肝癌、黑色素瘤和肺癌癌症。
FDA授予突破称号2020年药物治疗,患者治疗转移性asp。
这意味着药物已经加快发展符合FDA的标准和审查。去年,该机构授予孤儿药指定为软组织肉瘤atezolizumab一般来说,一个状态,为公司提供激励开发药物罕见疾病。
NCI的2期临床试验登记49个民族不同的患者2岁以上扩散的asp。病人有注入atezolizumab每21天。
大约三分之一的患者对治疗某种程度的肿瘤收缩。大多数的其他病人经历了稳定的疾病。
患者两年的治疗被给予一个机会休息治疗长达两年密切监测,根据这项研究。这些患者的疾病进展。
大约41%的患者接受了药物严重的副作用包括贫血、腹泻、皮疹、头晕、高血糖和四肢疼痛,但没有病人研究,因为副作用。
“这代表批准罕见疾病的胜利,这是本次在临床试验中,”陈说。“对于这个批准通过一种罕见的疾病,并且能够对这些年轻人的生活产生影响,是非常重要的。”
研究小组现在与atezolizumab进行额外试验病人asp。这包括药物结合其他疗法。
基因泰克,罗氏集团的成员和atezolizumab的制造商,提供了药物NCI通过研发合作协议。
更多信息:在波士顿丹娜-法伯癌症研究所拥有更多肺泡软部分肉瘤在孩子。
版权©2022每日健康。保留所有权利。