研究提供了对大脑疾病中异常蛋白质沉积结构的见解
凯斯西储大学医学院的科学家们已经确定了与卢伽雷氏病和其他神经退行性疾病有关的蛋白质“原纤维”的结构,这一发现为研究有毒蛋白质如何在大脑神经细胞之间聚集和扩散提供了线索。
他们的研究结果还可能导致开发治疗肌萎缩侧索硬化症(ALS)和额颞叶痴呆(FTD)等疾病的药物。
“这些毁灭性的大脑影响成千上万美国人的疾病在全球范围内呈上升趋势,而且没有有效的治疗方法来阻止它们的发展,”医学院生理和生物物理系教授、该研究的资深作者维托尔德·苏雷维奇说。
这项研究发表在3月12日的在线期刊上自然通讯。李秋野,系研究生,第一作者;凯斯西储医学院学生迈克尔·巴宾查克对此也有贡献。
这项研究得到了美国国立卫生研究院的支持。
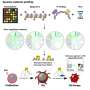
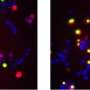
TDP-43通常是一种与核酸相互作用的可溶性蛋白质。然而,在一些神经退行性疾病中,这种蛋白质会形成巨大的、有害的绳状团块,积聚在患者的大脑中。
这些被称为淀粉样原纤维的异常结构是肌萎缩侧索硬化症(ALS;也被称为Lou Gehrig's病)和FTD,这是50多岁和60多岁的年轻人最常见的痴呆原因。
类似的TDP-43纤维结构也与其他脑部疾病有关,包括阿尔茨海默病和慢性创伤性脑病,这是一种由反复脑损伤引起的疾病,经常发生在踢足球和其他接触性运动的运动员身上。
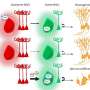
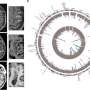
通过低温电子显微镜技术(低温电子显微镜),作者分析了数千张由TDP-43关键片段在试管中形成的原纤维图像。他们以接近单个原子的分辨率确定了这些细长结构的复杂结构。在其他发现中,这一结构洞察揭示了更多TDP-43拷贝可以锁定的模板的性质。
基于这一结构模型,研究人员还讨论了原纤维如何结构可以通过与ALS和FTD遗传形式相关的TDP-43氨基酸突变以及该蛋白的衰老依赖性修饰来控制。
“这确实是一个令人兴奋的进展,因为它揭示了这些有毒聚集体生长的机制,”李说。
“这反过来又为这些聚集体如何在受影响的大脑细胞之间传播提供了重要线索。”
“对由TDP-43形成的纤维结构的详细了解也可能导致治疗这些破坏性脑部疾病的药物的开发,”Surewicz说。
更多信息:自然通讯(2021)。DOI: 10.1038 / s41467 - 021 - 21912 - y