缺失的蛋白质促进了Mulibrey综合征患者的遗传不稳定

安达卢西亚分子生物学和再生医学中心(CABIMER)的研究人员与瑞士实验癌症研究所(ISREC)合作,研究了穆利布雷综合征患者更容易发展为肿瘤的机制。他们的结果指出了TRIM37蛋白的重要作用,其缺失解释了肿瘤细胞的外观。
mulibrey综合症是一个所谓的罕见的疾病因为每1万人中不到5人会得这种病。其中一些疾病通常有非常明确的遗传基础。因此,研究这些疾病患者中改变基因的分子功能,除了有助于寻找新的诊断和治疗方法,还有助于我们了解个体正常发展所必需的基本机制。
该疾病的特点是生长迟缓,心力衰竭问题和肝脏病理。此外,患者更有可能发展成某些类型的肿瘤。科学文献表明,这种疾病的发生与一种名为TRIM37的基因功能的缺失有关。然而,这种蛋白质所起的分子作用以及其功能的缺失如何导致疾病仍未解决。这项研究特别关注的是该基因功能的缺失可能如何影响穆里布里综合征患者的肿瘤发展。
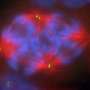
Trim37是泛素连接酶;一种能够通过添加称为泛素的小三种蛋白质来改变其他靶蛋白的蛋白质。该改性可以对目标蛋白质产生若干效果:从稳定和促进其突然触发其降解的功能。本研究由Fernando Romero Balestra(Cabimer / Us)的领导,与来自瑞士实验癌症研究所(ISREC)的一群人合作,其他研究人员来自安达卢西亚的分子生物学和再生医学中心(Cabimer)包括Pablo Huertas博士(Cabimer / Us),AndrésolmínguezCalvo(Cabimer / Us),以及CSIC研究员RosaM.Ríos控制名为Centrosomes的小细胞器的数量。Centrosomes参与了形成有丝分裂主轴所必需的微管的成核和组织,以及在细胞分裂期间遗传物质的正确隔离。健康细胞有两个中心,后细胞分裂,分布在两个子细胞之间,从而遗传一个Centrosome.每个。在进入下一个有丝分裂之前,每个子细胞必须通过复杂和高度调节的分子过程“构建”一种新的Centrosome,以保证单一的新中心组的形成,并确保在下一个有丝分裂中的染色体的正确分离。本研究描述了通过具有较高数量的中心的含有更多的CentroSomes,在细胞部门中形成异常染色的染色体和产生具有错误数量的染色体的细胞和产生细胞。
有趣的是,该中核数量和相关染色体隔离问题的这种失呼算法是许多肿瘤类型存在的特征。因此,研究人员表明Trim37作为中心数量调节剂的作用可能是Mulibrey综合征患者肿瘤形成的关键。但是如何将Trim37与形成新的CentroSomes连接的分子机制是什么?回答这个问题,研究转向分子生物学细胞生物学技术。为了表征这些新的中心体在缺乏TRIM37的细胞中不受控制地形成的机制,研究人员使用了容易在实验室中生长的人类细胞系,这些细胞系可以通过Crispr/Cas9基因组编辑技术或RNA干扰(RPE-1和HeLa细胞)进行修饰。
这些技术的使用揭示了Trim37的缺失如何通过迄今为止的中心组形成途径激活中心组形成,这取决于蛋白质环蛋白,PLK4,HSSA-6和PLK1。缺乏TRIM37诱导中心的形成,该结构用作不受控制的中心生产的平台。
这项研究的结果有助于更好地理解参与Mulibrey综合征的分子机制,并为寻找发展为肿瘤病理的Mulibrey综合征患者的个性化治疗打开了大门。未来,作者计划研究是否在其他肿瘤类型中,参与额外中心体形成的分子机制起关键作用。
进一步探索









用户评论