CRISPR微基因的方法停止基因小鼠的肝脏疾病

新CRISPR基因编辑技术防止基因肝脏疾病是由数百种不同的突变和改善临床症状的老鼠,宾夕法尼亚大学医学研究人员报道在新概念验证研究发表在科学的进步。调查结果显示一个有前途的CRISPR工具,可以治疗一种罕见的代谢尿素循环障碍引起的缺乏这种酶,鸟氨酸氨甲酰基转移酶(OTC),以及其他遗传性疾病引发的不同的相同基因的突变。
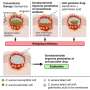
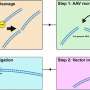
CRISPR方法构建了一个前一个发达的宾夕法尼亚大学医学这仅限于纠正只有一个突变,受益新生鼠而不是成年人。技术,使用了一个小说,双重腺相关病毒(AAV)提供其components-inserted“微基因”到场外的基因组完成持续表达肝细胞在所谓的“削减”和“粘贴”的方法。不纠正突变,而被添加到一套新的指令细胞。因此,研究人员观察到新生鼠的临床效益,持续到成年。
“像大多数遗传疾病在新生儿出现致命的影响,早期治疗是有效的长期是必不可少的,”James Wilson说,医学博士,博士,教授,医学、基因治疗项目主任和宾夕法尼亚大学的孤儿疾病中心。“在这里,我们搬CRISPR方法期待不仅维持细胞表达场外,还扩展工具的能力。我们的目标是最终将这种基因编辑方法从动物治疗场外障碍患者和其他遗传疾病引起的突变比一个单一的、分散在整个gene-rather主要突变。”
发现近40000年出生、场外障碍可以来自超过300种不同的基因突变在场外。由于这些突变发生在X染色体,这是典型的男性,而女性携带者。尿素循环是一系列的六个肝酶使机体的氨。这些酶缺失或不足时,血液中氨积累和传播到大脑,会导致脑损伤,甚至死亡。治疗疾病,患者服用药物来刺激替代氮间隙通道,或在严重的情况下,肝脏移植手术。然而,这些患者的死亡率仍然很高,因此需要新的、更有效的治疗方法。
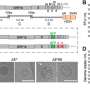
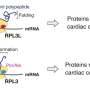
开发一个广泛适用的基因编辑工具,团队构建了一个新的双AAV载体包含RNA-guided细菌蛋白质被称为Cas9-a快速而可靠的方法和操作基因在细胞。被称为AAV8,这个Penn-developed向量专门为肝细胞有亲和力。第二AAV包含一个功能完备的“微基因”表达了人类OTC-the捐赠DNA-driven codon-optimized肝脏特异性启动子,以确保它只表达在肝细胞注入血液。
第一步是创建一个打破的DNA Cas9沿着基因在目标站点上(“削减”),为增加微基因奠定了基础的称为同源修复,或HDR(“粘贴”)。
”与其他CRISPR方法删除或修改正常基因的一部分,这种技术集成了一个新的部分,”第一作者说丽丽Wang博士,医学研究助理教授。“我们不是要正确突变阻止肝细胞生产场外,我们添加这个新的微基因的细胞可以。”
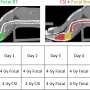
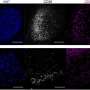
老鼠接受目标向量显示25 - 35%的OTC-expressing 3和8周细胞在肝脏,这四次和3倍高于处理没有针对性的老鼠向量。在两个时间点(3和8周),大多数OTC-positive肝细胞是位于集群分散在所有部分有针对性的老鼠的肝脏。
研究人员还发现氨含量减少60%目标比未经处理的小鼠老鼠美联储高蛋白饮食,临床迹象表明肝细胞生产出了场外。
“与这些成功的动物研究中,我们已经接近一个潜在的“广谱”基因编辑方法治疗场外缺乏症患者,无论突变和临床状态,”威尔逊说。“通过额外的临床前研究,下一步是找到一个安全港网站在人类基因肝细胞,然后测试类似的基因编辑方法。”
更多信息:“mutation-independent CRISPR-Cas9-mediated基因打靶的方法治疗的小鼠模型鸟氨酸氨甲酰基转移酶缺陷”科学的进步(2020)。advances.sciencemag.org/content/6/7/eaax5701