药物通过抑制蛋白质的产生来抑制致命的肝癌
在实验室实验中,加州大学旧金山分校的研究人员使用一种令人惊讶的新方法成功地击退了侵袭性肝癌的生长。传统上,靶向癌症治疗的目的是使携带癌症驱动基因的蛋白质失效。相反,UCSF的科学家们从一开始就阻止了这些蛋白质的生成,包括那些保护肿瘤免受免疫系统攻击的蛋白质。
正如在自然医学2019年1月14日,通过使用遗传方法和目前正在临床试验中的药物直接抑制翻译(遗传物质转化为蛋白质的细胞过程),研究人员不仅能够减缓肿瘤在一种新的环境中的疯狂生长小鼠模型肝癌症还能阻止癌症逃避免疫反应的能力。
“这是肝癌干预的新途径,”该研究的资深作者Davide Ruggero博士说,他是癌细胞如何破坏正常细胞的专家蛋白质合成刺激自己的成长和生存。“有一种特殊的蛋白质子集,对癌细胞更有益正常细胞它被称为“癌症蛋白质组”。一旦我们知道细胞转向支持该蛋白质组的机制,我们就可以开发针对它的药物。”
原发性肝癌或肝细胞癌是全球癌症死亡的第二大原因,每年造成60万人死亡。如果肿瘤仍然局限于肝脏,大约三分之一的这些癌症在早期阶段是可以治疗的。但是,当肝癌扩散到其他器官时,5年生存率会急剧下降,而很少有靶向治疗可以减缓其扩散。
一种很有前途的治疗方法是癌症免疫疗法,它可以释放人体的免疫系统去除肿瘤。免疫疗法发展的关键是发现许多癌症通过披上被称为“检查点”蛋白质的聪明分子伪装来逃避免疫攻击。例如,侵袭性肝癌细胞将自己包裹在一种名为PD-L1的检查点蛋白上,这种检查点蛋白会进入免疫细胞表面的一种名为PD-1的受体,并有效地将它们“关闭”。
有一类免疫治疗药物叫做检查点抑制剂,它可以阻断检查点蛋白,使肿瘤可见并容易受到攻击。但阻断PD-L1的药物atezolizumab (Tencentriq)尚未对治疗侵袭性肝癌有效。Ruggero实验室的这项新研究提供了一种破解癌症防御的替代策略——如果检查点蛋白从一开始就不存在,那么它们就不需要被阻断。
侵袭性肝癌依赖于增强的蛋白质合成
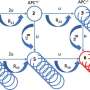
细胞生成蛋白质分为两个阶段:转录和翻译。在转录过程中,编码在DNA中的遗传指令被复制,存储在一种叫做RNA的新分子中,并被发送到细胞中来指导翻译过程——由称为核糖体的细胞机器组装蛋白质。科学家们通常认为,由特定基因产生的RNA的数量是由该基因产生多少蛋白质的合理指标。但Ruggero之前的研究和这项新研究表明,在包括侵袭性肝癌在内的许多癌症中,这种假设是极不正确的。
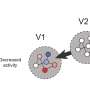
在这项新研究中,Ruggero的团队使用了一种新开发的小鼠模型来研究主要由致癌基因驱动的肿瘤之间RNA和蛋白质产生的差异喀斯特前者生长缓慢,往往不会转移,而后者则是由这两种因素导致的更致命的肿瘤喀斯特第二种致癌基因叫做MYC.后一种癌症在一定程度上是通过逃避免疫系统的监视而迅速生长并迅速扩散到全身。
奇怪的是,尽管两人的行为有着深刻的差异肿瘤基因分析显示,两种癌症的DNA转录的RNA序列大致相同,数量相同。那么,为什么要这么做呢MYC/喀斯特肿瘤生长更加凶猛,转移和显著降低生存率?
为了回答这个问题,Ruggero的团队采用了一种10年前的技术,称为核糖体分析,由UCSF生物化学家Jonathan Weissman博士开发,该技术允许他们对两种肿瘤类型的核糖体蛋白质工厂中正在积极构建的所有蛋白质进行快照。通过比较核糖体上被转录的RNA和实际被翻译成蛋白质的RNA,研究人员发现了两者之间的明显差异喀斯特而且MYC/喀斯特巨蟹座:简而言之,就是巨蟹座MYC致癌基因直接劫持细胞的翻译机制,为自己构建一个更致命的癌症蛋白质组。
“在癌细胞中有转录基因并不意味着你会得到蛋白质产物。这是一个关键点,我们越来越开始认识到我们必须如何看待癌症中基因表达的变化。”Ruggero说。
然而,这篇论文最引人注目的发现之一是喀斯特而且MYC/喀斯特肿瘤具有几乎相同水平的编码PD-L1的转录RNA,越具有侵略性MYC/喀斯特肿瘤产生大量的PD-L1蛋白。这一发现表明喀斯特肿瘤在一定程度上暴露在免疫系统的愤怒之下,MYC/喀斯特肿瘤能够通过劫持蛋白质翻译来将自己隐藏在更强大的PD-L1隐身斗篷后面,从而更快地扩散。
作者预测,随着PD-L1的减少,MYC/喀斯特肿瘤同样容易受到免疫攻击喀斯特肿瘤。为了验证这一想法,他们转向了一种正在进行二期临床试验的新药物,这种药物可以消除免疫系统对这些癌症的保护。
攻克癌症的“蛋白质成瘾症”
Ruggero的大部分职业生涯都致力于强调癌细胞如何劫持翻译控制,以及直接针对癌症对高水平蛋白质合成的“上瘾”的治疗方法的潜力,同时不影响健康细胞(蛋白质胃口明显较低)。
例如,在一个2015年研究成果鲁杰罗的研究小组发现,经过基因改造后,小鼠体内细胞产生蛋白质的能力只有正常水平的一半,它们的发育完全正常。然而,这些小鼠对癌症有很强的抵抗力,因为癌细胞无法产生大量生长所需的特定蛋白质。最近的一项研究Ruggero实验室的研究人员发现,一种侵袭性前列腺癌可以通过使其在失控的蛋白质生产需求下“燃烧”而成为靶标。
2013年,Ruggero和UCSF的同事Kevan Shokat博士成立了圣地亚哥的eFFECTOR Therapeutics, Inc,以探索专门针对蛋白质翻译的药物是否可以形成一类新的抗癌化合物的基础。
这项新研究测试了一种名为eft508的eFFECTOR化合物(通过抑制一种名为eIF4E的细胞“翻译因子”来减少蛋白质的产生,eIF4E负责将RNA分子与核糖体配对)是否能阻止肝癌隐藏自己不被免疫系统发现。
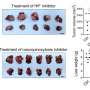
研究人员提供了目前处于第二阶段的实验性药物临床试验为了测试它对几种癌症的疗效,他们对模型小鼠进行了实验,发现每种癌症对治疗的反应都不同。喀斯特eFT508治疗对小鼠没有影响,可能是因为它们的肿瘤不那么严重依赖选择性蛋白质合成。但是在老鼠身上MYC/喀斯特在肿瘤中,每日剂量的eFT508使肿瘤细胞中的PD-L1蛋白水平减半。这些接受治疗的小鼠体内的免疫细胞很快开始攻击它们的肿瘤,它们的存活率显著提高。
“PD-L1 RNA翻译成蛋白质刺激癌症免疫逃避,但也使癌细胞更容易受到翻译抑制剂的新型抗肿瘤疗法的影响,”博士后研究员徐一晨博士说,他是这项新研究的主要作者之一。
除了PD-L1,MYC/喀斯特上调与癌症有关的其他几个关键蛋白质的翻译细胞繁殖、逃避免疫系统和在器官间传播的能力。这意味着,除了像传统免疫疗法那样抑制检查点蛋白外,科学家们现在的目标可能是阻止许多蛋白质的增强生产癌症细胞依赖于以高度选择性的方式治疗侵袭性癌症。
Ruggero说:“如果侵袭性肝癌依赖于这种增加的转译,如果你用转译抑制剂打击它,它可能会死亡。”“这是一场新兴运动的基础癌症治疗."
进一步探索