Nature, Structure上的HIF-2的研究
对新型HIF抑制剂恢复对缺氧反应控制的潜力的新见解-代表了一种新的抗癌策略的潜在基础-是最近发表的文章的焦点自然而且结构纽约市立大学高级科学研究中心(CUNY ASRC)的凯文·加德纳的研究成果。
这项研究始于加德纳在德克萨斯大学西南医学中心工作期间,目前正在进行肾癌治疗的临床试验。这些新出版物——包括来自纽约市立大学ASRC、德克萨斯大学西南医学院和Peloton therapeutics的研究人员——证明了Peloton开发的化合物在更复杂的肾癌模型中是有效的。
加德纳说:“几乎所有参与生物医学研究的人都梦想着自己的发现能走出实验室,进入临床。”bob88体育平台登录“这些论文代表了这一飞跃的关键组成部分,展示了一项基础科学发现如何转化为抑制患者源性肿瘤系统中肾癌的基础。”
这篇文章发表在自然9月5日的重点是缺氧诱导因子(HIF)系统,这是一个20多年来已知的途径,参与正常细胞对低氧(缺氧)的适应,并在肾癌类型中被征用。HIF-2系统最初是由德克萨斯大学西南分校的研究人员Steven McKnight和David Russell在20世纪90年代中期克隆的,作为一种在低氧条件下激活基因表达的转录因子。由于在细胞内靶向和抑制这种蛋白质的技术挑战,HIF-2系统通常被认为是不可用的,就像其他细胞内的非酶靶一样。
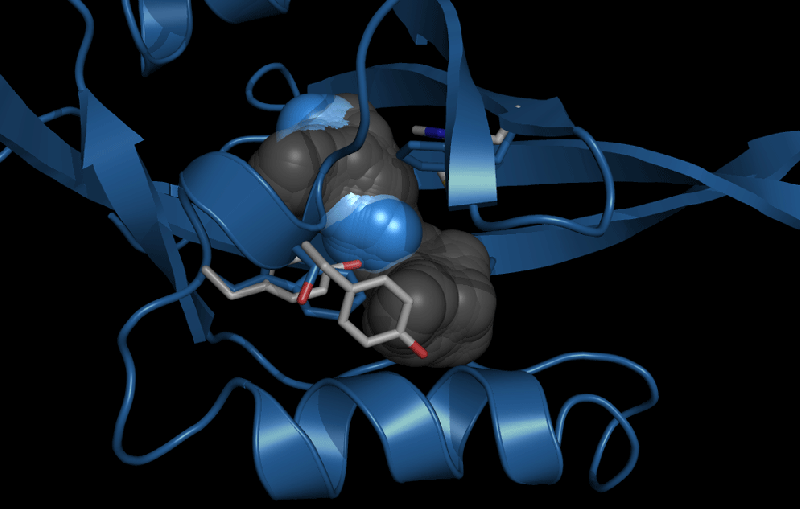
然而,Gardner的研究揭示了HIF-2的HIF-2a成分含有一个大的内腔,这可能是药物类分子的良好结合位点。加德纳和他在德克萨斯大学西南分校的同事理查德·布里克(Richard Bruick)一起利用了这一特点,利用高通量筛选发现了这类化合物,并通过体外生物物理和生化实验证明了它们的功效。
这项研究后来被授权给生物技术初创公司Peloton Therapeutics,该公司已经将德克萨斯大学西南分校团队进行的学术工作推进到目前正在临床试验中作为治疗方法的新型化合物肾癌.
虽然这项工作的某些方面已经进入了临床翻译,但关于HIF-2是如何工作的,仍然存在一些基本的问题。与自然文章中,Gardner对HIF-2的HIF-2a组分的持续学术研究是即将发表的一篇文章的重点结构,也有费尔南多博士Corrêa,共同第一作者的文章和前高级研究员在城市大学ASRC的结构生物学倡议。
其中一个关键方面是HIF-2a药物结合腔打破了许多控制蛋白质通常如何折叠和功能的传统规则。了解空洞在没有化合物的情况下是如何保持开放的,以及它是如何对人造和天然配体做出反应的,为蛋白质通常如何对环境变化做出反应提供了新的见解。
为此,加德纳团队与蛋白质设计界的专家合作,重新包装了HIF-2a的内部,重塑了结合位点,并有效地用蛋白质组填充腔体,而不是药物。正如即将报道的结构文章(Corrêa, Key, et al., 2016),这些周围的蛋白质适应这些对结构和动力学有一系列影响的修饰。
Gardner说:“这项工作让我们深入了解了这种配体结合腔的蛋白质折叠的基本规则,为我们设计新型蛋白质传感器提供了线索,这些传感器可以响应细胞信号并控制我们选择的输出。”