实时成像显示,通过改变肿瘤微环境可以提高对癌症药物的反应
冷泉港实验室(CSHL)的科学家说,通过引入改变癌细胞与其周围环境(称为肿瘤微环境)相互作用的药物,应该有可能显著改善常见癌症对现有“经典”化疗药物的反应。
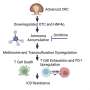
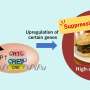
在今天在线发表在杂志上的研究中癌症细胞, CSHL助理教授Mikala Egeblad和她的团队使用“live”进行报告显微镜观察一下癌症细胞小鼠肿瘤对广泛使用的化疗药物有反应阿霉素.他们发现选择性抑制两种因素调节肿瘤微环境酶叫做基质金属蛋白酶(基质金属蛋白酶)和一类被称为趋化因子的免疫信号分子乳腺肿瘤老鼠对药物反应更灵敏。
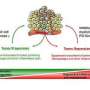
众所周知基因突变而且表观遗传变化在癌细胞中,肿瘤具有抵抗治疗的能力。但是,除了癌细胞之外,肿瘤还包含许多其他细胞,令人惊讶的是,我们对这些非癌细胞(构成肿瘤微环境的“基质”细胞)分泌的因子如何影响耐药性知之甚少。这些细胞包括白细胞,其中一些是炎症细胞。
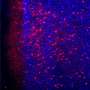
Egeblad的团队使用实时显微成像技术来详细研究癌细胞在不同肿瘤微环境下对阿霉素的反应。由此产生的延时电影揭示了药物如何流经和流出血管,滋养肿瘤;药物在不同进展阶段肿瘤中杀死癌细胞的方式和速度;以及肿瘤细胞与周围基质组织之间相互作用的动态,在给药前,期间和之后。
“我们能够清楚地看到,微环境对药物反应起着至关重要的作用,”埃格布莱德说,“特别是通过调节流经肿瘤和周围血管的渗透性或‘渗漏性’,以及影响炎症细胞的局部招募。”
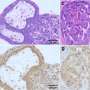
在显微镜下观察时,发现对阿霉素的耐药性与肿瘤分期有关。在给药后持续观察肿瘤,发现这种反应与血管将阿霉素运送到癌细胞的能力相关,相对而言,这种反应不是在早期或晚期,而是在肿瘤发展的中期表现最好。
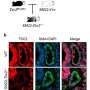
根据埃格布莱德的说法,被改造成缺乏编码MMP9酶的基因的小鼠,“血管明显更容易泄漏,这与对阿霉素的更好反应惊人地对应”。MMP9酶有助于调节血管的渗透性。
她指出,现有的MMP酶化学抑制剂在临床试验中失败了。“但我们的数据表明,这些或其他影响血管通透性的药物可以用于对化疗产生更好的反应。”
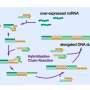
从CSHL团队的实时成像中收集到的另一个重要发现是,髓系细胞——肿瘤中最常见的非癌细胞之一——在化疗期间一直被招募到肿瘤部位[视频剪辑待发布]。骨髓细胞倾向于被吸引到细胞死亡的地方。研究小组发现,这种被称为趋化性的吸引力是CCL2激活信号的结果,CCL2是一类免疫细胞招募分子(称为趋化因子)的成员。
通过敲除这种趋化因子的受体编码基因(称为CCR2),研究小组能够减少髓系细胞向肿瘤的募集。重要的是,这也导致对阿霉素和另一种常用化疗药物顺铂的反应显著改善。这一观察结果很重要,因为它指出了一种可能提高化疗药物杀死癌细胞效果的新方法。
CSHL团队现在的目标是通过确定在化疗期间被招募到肿瘤的髓系细胞如何促进癌细胞对药物治疗的反应,来找到更多的方法来促进化疗反应。