1型糖尿病:保持肠道酶ACE2防止糖尿病患者失明
在美国成年人致盲的主要原因是糖尿病性视网膜病变,逐渐损害血管的光敏组织的眼睛。然而这种伤害的来源似乎在于belly-mainly漏水的小肠,削弱了肠道细菌之间的障碍和血液系统,根据一项研究发表在杂志上循环的研究。
研究血液人类被试1型糖尿病患者和1型糖尿病小鼠模型被用来探索机制糖尿病视网膜病变。结果显示,可能可以预防,甚至扭转,眼睛损伤。
“据我们所知,本研究是第一次肠道屏障的破坏与糖尿病视网膜病变的发病机制,也直接链接肠漏与1型糖尿病视网膜病变严重程度在人类受试者,”玛丽亚·格兰特说,医学博士教授,研究小组的领导人,在伯明翰阿拉巴马大学眼科及视觉科学。
一些背景知识理解格兰特的研究是很有用的。
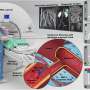
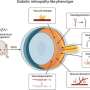
首先,众所周知,1型糖尿病就是说系统性肾素-血管紧张素系统,或RAS。RAS系统调节血压的激素和酶和其他代谢变化。除了系统性RAS,也有局部RAS网络在不同组织行动。一个关键的RAS酶ACE2,或血管紧张素转换酶2。ACE2的损失在糖尿病激活vasodeleterious RAS轴,减少vasoprotective RAS轴。有趣的是,在1型糖尿病小鼠模型,用修改后的肠道喂养老鼠的乳酸菌菌株paracasei,工程生产人类ACE2,保护小鼠免受糖尿病视网膜病变进展。最后,缺乏ACE2在肠道,肠道通透性增加和系统性炎症。
人类的研究,发表在循环研究1型糖尿病患者相比,与控制。1型糖尿病的受试者进一步分层为三组:糖尿病视网膜病变,non-proliferative糖尿病视网膜病变和更严重的疾病称为增生性糖尿病性视网膜病变。通过测量血液中的某些免疫细胞和生物标志物水平,包括肠道微生物抗原,研究人员发现,人体与视网膜病变提供系统性RAS和深刻的肠道通透性缺陷激活组件的适应性和先天免疫反应。此外,增加糖尿病性视网膜病变的严重程度被发现与水平的提高肠道通透性生物标志物和肠道微生物抗原。这包括增加血管紧张素ⅱ水平,RAS激活vasodeleterious RAS轴激素。
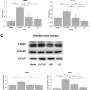
使用1秋田的鼠标类型糖尿病模型,研究人员首先给ACE2-producing乳酸菌paracasei,由Qiuhong Li博士,来自佛罗里达大学的,口头的老鼠开始在糖尿病的发病。这种益生菌治疗预防肠道上皮ACE2的损失通常出现在秋田老鼠,而且重要的是,它阻止肠道上皮和内皮屏障损伤。它还降低了高血糖水平称为高血糖。
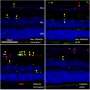
口服ACE2-producing乳酸菌paracasei治疗时扣留,直到六个月后糖尿病成立,延迟治疗逆转肠道屏障功能障碍和已经形成的小鼠糖尿病性视网膜病变,包括减少视网膜受损的毛细血管的数量。
格兰特和他的同事们还发现几个机制,导致了ACE2-reduced肠道屏障损伤和ACE2-lowering血糖。验证结果的秋田犬/ ACE2-producing乳酸菌paracasei模型,他们创造了第二个模型(一个转基因秋田犬应变,过表达人类ACE2在小肠上皮细胞。
”工作的重要性,我们表明,肠道RAS特异表达导致易位的肠道微生物抗原进入等离子体,”格兰特说。“这些细菌肽通过toll样受体激活内皮,创建一个炎症内皮一直强烈与血管疾病的发病机制,包括糖尿病性视网膜病变。
“我们证明了人体肠道屏障功能的损失1型糖尿病使用肠道屏障生物标志物,这增加渗透率与gut-derived免疫细胞激活。”
更多信息:拉姆et al,维护肠内ACE2防止在1型糖尿病,糖尿病性视网膜病变循环研究(2022)。DOI: 10.1161 / CIRCRESAHA.122.322003