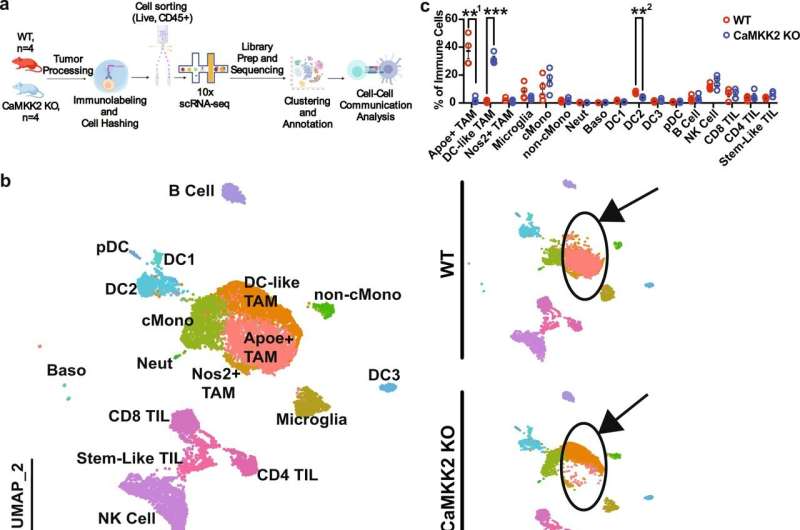
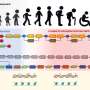
胶质瘤微环境中的促肿瘤免疫编程依赖于CaMKK2。描述scRNA-seq实验设计的示意图。n = 4 WT和CaMKK2 KO小鼠原位植入50k CT2a。在D14切除肿瘤并进行肿瘤处理。样本用Live-Dead活性染料、CD45和TotalSeqB抗小鼠Hashtag抗体标记。对CD45+活细胞进行分类,然后按基因型将其按等量混合。图片由BioRender.com创建。b 14k CD45+活免疫细胞从WT和CaMKK2 KO荷瘤半球D14 p.i上进行分类。使用10X平台制备HTO和基因表达文库。使用无监督聚类方法识别的细胞类型的UMAP图显示了聚集数据集,并按基因型分层。c通过scRNA-seq鉴定的大量免疫细胞类型。 n = 4 per genotype, two-way RM ANOVA p < 0.05 with post hoc unadjusted two-tail Fisher LSD t-test. **1p = 0.0059, ***p = 0.0003, **2p = 0.0016. Data are presented as mean ± SEM. d Dot plots corresponding to the cell types displayed in the UMAP plots show expression of subset-specific genes, with the dot size representing the percentage of cells expressing the gene and the color representing its average expression within a cluster. Credit:自然通讯(2022)。DOI: 10.1038 / s41467 - 022 - 34175 - y
杜克大学健康中心的研究人员发现了致命脑肿瘤环境中的一个独特过程,该过程会导致对免疫增强疗法的抵抗,并可以靶向促进这些药物的效果。
这一发现发表在自然通讯,解释了恶性胶质瘤的一个棘手问题。恶性胶质瘤是一种致命的脑肿瘤,众所周知,它是不受影响的免疫检查点抑制剂这是一种对其他癌症非常有效的免疫疗法。
“传统上,研究人员通过观察免疫治疗和耐药性癌症细胞寻找攻击靶点,或通过探索肿瘤环境寻找潜在的改善途径免疫反应主要作者威廉·h·托马泽夫斯基博士说,他是杜克大学神经外科的博士候选人,进行了这项研究。“我们在这项工作中的方法是找到环境因素这可能会使胶质母细胞瘤更容易受到免疫疗法的影响。”
Tomaszewski和他的同事——包括资深作者、医学博士、神经外科学教授John Sampson——专注于一种被称为钙调素依赖性激酶激酶2 (CaMKK2)的分子,它存在于神经元和神经细胞中免疫细胞.这种分子在恶性胶质瘤环境中的癌症支持细胞中高度活跃,与人类较差的生存率有关。
在小鼠研究中,在CaMKK2水平高的动物体内,癌症杀伤t细胞被抑制攻击脑肿瘤细胞。在没有CaMKK2的小鼠中,t细胞仍然是侵略性的癌症杀手。
CaMMK2不仅影响t细胞的功能,而且这种蛋白质还改变了巨噬细胞的行为,使这些免疫细胞对t细胞的帮助减少。在这里,当CaMMK2被消除时,巨噬细胞有助于肿瘤的杀伤。
一个令人惊讶的发现是CaMKK2,特别是在神经元中,支持脑肿瘤的生长并抑制免疫系统的功能。了解神经元如何做到这一点可能会在未来确定更多的治疗靶点。
因为CaMKK2在肿瘤支持中高度表达神经元和巨噬细胞,研究人员说,它促进对免疫检查点抑制剂药物的抵抗,关闭细胞刹车,加速t细胞的抗癌能力。
“当没有CaMMK2的小鼠接受检查点抑制剂治疗时,它们有反应,存活时间更长,但有CaMKK2的小鼠则没有,”Tomaszewski说。“这表明CaMKK2是一个潜在的治疗靶点。如果我们能够抑制CaMMK2,我们就可能释放出对其他癌症有益的免疫治疗药物的力量,但对胶质母细胞瘤无效。”
更多信息:William H. Tomaszewski等人,神经元CaMKK2促进胶质母细胞瘤免疫抑制和检查点封锁抵抗,自然通讯(2022)。DOI: 10.1038 / s41467 - 022 - 34175 - y
期刊信息:自然通讯
所提供的杜克大学