老年痴呆症药物试验显示“持续改善的证据”
大约40年前,阿伯丁大学心理健康(临床)主任克劳德·威奇克教授取得了突破性进展,他发现与阿尔茨海默症相关的神经纤维“缠结”是由一种tau蛋白构成的。
自那以后,他致力于研究针对并“溶解”这些缠结的治疗方法,他认为这是减缓甚至停止阿尔茨海默症的关键,阿尔茨海默症影响着全球数百万人的生活。
这项最初的研究始于威奇克教授在剑桥的时候,并在1997年他搬到阿伯丁大学时继续进行。五年后,阿伯丁大学成立了一家名为TauRx Therapeutics的公司,将这项有前途的研究转化为临床。
在Wischik教授的领导下,该公司继续专注于基于tau的阿尔茨海默症研究,与此形成鲜明对比的是,许多其他研究方法都专注于该疾病淀粉样斑块——在阿尔茨海默症患者的大脑中发现的第二个病变。该公司继续与阿伯丁大学(University of Aberdeen)合作,主要研究设施和运营基地设在阿伯丁,公司总部设在新加坡。
10月6日,TauRx宣布了名为LUCIDITY的三期临床试验的结果。
该试验比较了服用该公司口服药物甲磺酸氢甲基硫氨酸(HMTM) (Tau蛋白聚集病理的有效抑制剂)与服用对照剂(MTC)的不同阶段阿尔茨海默氏症患者的结果,并与历史对照和其他可用的基准数据进行比较。
TauRx报告:
- 对于早期阿尔茨海默氏症(MCI)患者,HMTM治疗导致认知能力比治疗前基线持续改善,脑萎缩恢复到与健康个体相似的水平
- 对于轻度到中度阿尔茨海默氏症患者,与历史匹配的阿尔茨海默氏症患者相比,HMTM稳定了认知和功能,并降低了脑萎缩率
TauRx断言:
- 来自LUCIDITY试验的数据首次提供了证据,证明AD在早期临床可检测阶段的持续改善和在更严重阶段的疾病进展稳定。
- 数据表明Tau蛋白是一个可行的一线治疗靶点,这与Tau蛋白病理开始于临床症状出现至少20年之前的证据一致。
- 对于患者来说,这意味着在早期阶段进行干预的可能性,在认知和功能下降这会导致丧失独立性。
关于当前数据分析的结果,Wischik教授解释说:“这是第一次有证据表明,在阿尔茨海默病(AD)的早期临床可检测阶段,持续18个月的个人治疗前基线的持续改善,以及在更严重阶段疾病进展的稳定。
“AD的结果证实了两项早期HMTM三期试验公布的结果。可获得的口服治疗不需要对常规临床护理进行昂贵的监测,这为在导致丧失独立性的认知和功能衰退开始之前进行干预提供了机会。
“这种疾病的Tau病理现在被认为是治疗的一个重要靶点,令人鼓舞的是,在这种疾病的早期阶段,使用靶向Tau的药物可以看到认知能力的改善。该领域主要关注淀粉样蛋白作为早期干预的靶点。我们的数据与Tau蛋白病理在临床症状出现前至少20年开始的证据一致,是一个可行的一线治疗靶点。”
该试验没有报道与治疗相关的严重不良事件或淀粉样蛋白相关成像异常(ARIA)的证据。
TauRx现在将使用来自试验的数据来支持监管提交。为了协助下一阶段的工作,该公司已在英国、美国和加拿大任命了战略监管顾问。TauRx计划在2023年将HMTM提交给英国、美国和加拿大的监管机构批准,其他地区也将跟进。
研究结果还将在2022年11月30日星期三在旧金山举行的阿兹海默病临床试验(CTAD)会议上发表。
第三阶段试验的进一步细节
甲磺酸氢甲基硫氨酸(HMTM)是一种口服Tau蛋白聚集病理的有效抑制剂。第三期LUCIDITY研究比较了HMTM 16 mg/天与甲基亚硫氯化铵(MTC)的剂量为4 mg,每周两次,以防止潜在的尿变色引起的偏差的最低要求。这项研究在598名AD严重程度从轻度认知障碍(MCI)到中度疾病阶段的患者中进行。
TauRx已经完成了第一个为期12个月的双盲试验阶段。第二个12个月的开放标签期正在进行,在此期间所有参与者都接受HMTM 16毫克/天。所有参与者都被要求淀粉样pet扫描呈阳性,并且不接受标准的AD对症治疗。
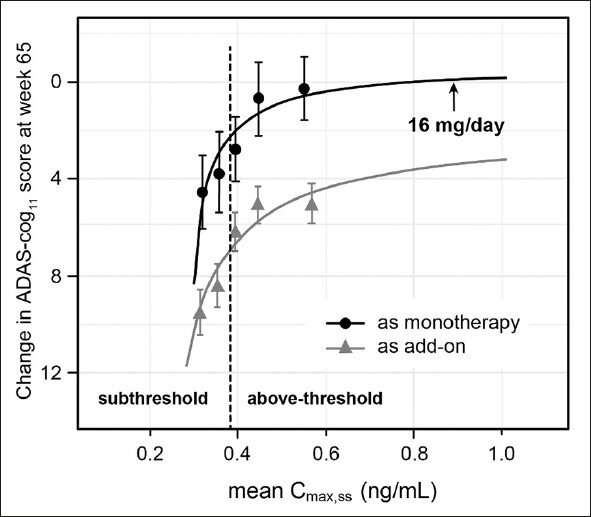
在那些每周两次接受MTC 4毫克的患者中,大多数人的血液活性药物水平超出了产生临床效果所需的阈值。在缺乏真正的安慰剂的情况下,设计的试验无法确定与预先指定的治疗无效安慰剂相关的主要临床终点的结果。根据现有的证据,TauRx不相信一个有效的具有临床终点的HMTM的安慰剂对照盲法试验在技术上是可行的。因此,TauRx分析了药物血药浓度与治疗效果之间的关系、治疗前基线的变化,以及与来自阿尔茨海默氏症神经成像计划(ADNI)的密切匹配数据的历史对照的比较。
从MCI到中度疾病的研究人群的总体基线MMSE评分为21。在最初的12个月里,接受16 mg/天剂量的参与者在共同认知和功能终点(1.3 ADAS-cog11单位和-1.0 adas - adl23单位)上的下降都很小。未经治疗的人群在12个月内的预期下降将在两个量表上约5个单位。
在接受16 mg/天剂量的105名MCI(基线MMSE评分23)参与者中,在ADAS-cog13量表上,在6个月(p=0.0002)、12个月(p=0.0391)和18个月(p=0.0473)时,认知能力比治疗前基线提高了2个单位,具有统计学意义。在6、12和18个月时,adc - adl日常生活亚量表工具活动的平均变化也高于治疗前基线。
147名轻度至中度AD患者(基线MMSE 20)每天服用16 mg,在前9个月出现2.5单位认知能力下降,在接下来的9个月没有进一步下降。ADCS-ADL量表的功能下降在12个月时为-2个单位,在18个月时为-3个单位,相对于发表的一项针对轻度至中度AD的历史试验中公开可用的安慰剂下降数据的meta分析,下降减少了约75%。
通过比较接受16 mg/天剂量的受试者与在年龄和临床严重程度上与研究人群最接近的ADNI受试者,证实了以认知功能变化(p=0.0008)和脑萎缩(p<0.0001)衡量的疾病进展有统计学意义的降低。在MCI和AD亚组中,差异仍具有统计学意义。正如预期的那样,患有MCI的LUCIDITY试验参与者在进入研究时,比ADNI健康的老年受试者有更多的脑萎缩,并且与ADNI MCI受试者一致。接受HMTM 16 mg/天治疗的患者脑萎缩的进展率明显低于ADNI MCI受试者(p<0.0001),与ADNI健康老年受试者的进展率相当。
相关研究也发表在阿尔茨海默病预防杂志.