FDA批准SPEVIGO用于广泛性脓疱性银屑病发作
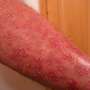
美国食品和药物管理局(fda)批准SPEVIGO (spesolimab-sbzo)作为成人广泛性脓疱性银屑病(GPP)发作的首选治疗方案。
SPEVIGO是一种新型的选择性抗体输注,可阻断白细胞介素-36受体的激活,该受体是免疫系统信号通路的一部分,被认为与GPP的原因有关。批准是基于12周的试验,其中53病人GPP耀斑患者接受SPEVIGO或安慰剂治疗。一周后,接受SPEVIGO治疗的患者比接受安慰剂治疗的患者没有出现明显的脓疱(54%比6%)。
在服用SPEVIGO的患者中最常见的不良反应(≥5%)是乏力和疲劳,恶心和呕吐,头痛,瘙痒和瘙痒,注射部位血肿和淤青,和尿路感染.
“GPP耀斑会极大地影响患者的生活,并导致严重的、危及生命的并发症,”该试验的首席研究员Mark Lebwohl医学博士在一份声明中说。“SPEVIGO的批准对皮肤科医生和临床医生来说是一个转折点。”
SPEVIGO的批准被授予勃林格殷格翰。
更多信息:
FDA的批准
版权©2022每日健康.保留所有权利。
引用: FDA批准用于广泛性脓疱性银屑病发作的SPEVIGO(2022年,9月7日),于2022年9月23日从//www.pyrotek-europe.com/news/2022-09-fda-spevigo-pustular-psoriasis-flares.html获得
本文件受版权保护。除用于个人学习或研究的公平交易外,未经书面许可,不得转载任何部分。内容仅供参考之用。