研究保存了小鼠的记忆,为主动免疫对抗阿尔茨海默病提供了有希望的新基础
在动物模型实验中,堪萨斯大学的研究人员发现了一种可能的免疫对抗阿尔茨海默病(AD)的新方法。
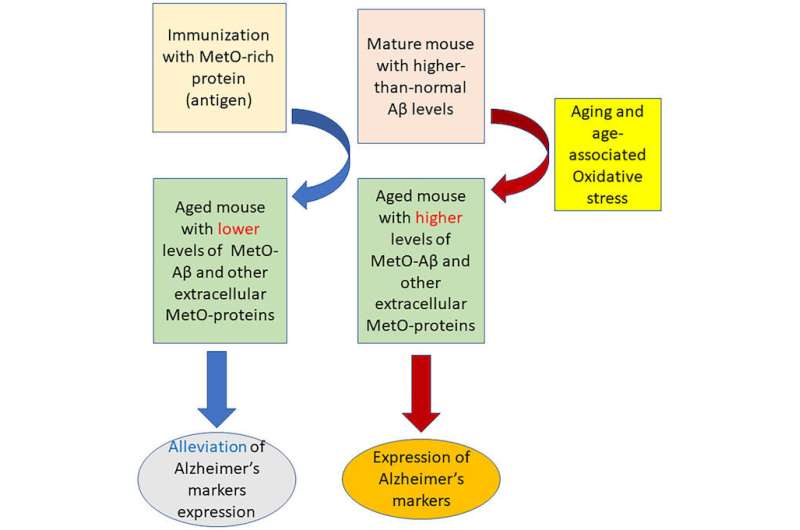
他们的方法使用了富含蛋氨酸的重组蛋白蛋白质从玉米中提取,然后在体外氧化产生抗原:富含蛋氨酸亚砜(MetO)的蛋白质。这种抗原被注射到体内后,会刺激免疫系统产生对抗β -淀粉样蛋白MetO成分的抗体,这种蛋白质对脑细胞有毒,被认为是阿尔茨海默病的标志。研究结果刚刚发表在同行评议的开放获取期刊上抗氧化剂.
堪萨斯大学药学院药理学和毒理学副教授、首席研究员Jackob Moskovitz说:“随着我们年龄的增长,我们有更多的氧化应激,然后β -淀粉样蛋白和其他蛋白质积累并被氧化和聚集——这些蛋白质抵抗降解或移除。”“在2011年发表的一项研究中,我给阿尔茨海默病的小鼠模型注射了类似的富含蛋氨酸亚硫酸钠的蛋白质,结果显示海马体中的淀粉样斑块负担减少了30%左右,海马体是阿尔茨海默病损伤发生的主要区域。”
Moskovitz用于ad模型小鼠接种的富含meto的蛋白质能够促使免疫系统产生针对含有meto的蛋白质的抗体,包括含有meto的β -淀粉样蛋白。引入以玉米为基础的富含MetO的蛋白质(抗原)可以促进人体的免疫系统产生和部署针对先前耐受的含有MetO的蛋白质(包括MetO- β -淀粉样蛋白)的抗体,并最终降低大脑中有毒形式的β -淀粉样蛋白和其他可能的蛋白质的水平。
在新的后续研究中,Moskovitz和他的合著者将富含meto的蛋白质注射到4个月大的ad模型小鼠中,这些小鼠经过基因改造,患上了家族性阿尔茨海默病。随后的测试表明,这种方法刺激小鼠的免疫系统产生抗体,可以缓解老年(10个月大的小鼠)AD表型的存在。
作者说:“这种治疗诱导了血浆中抗meto抗体的产生,这种抗体在至少10个月大的时候都表现出显著的滴度。”
莫斯科维茨在堪萨斯大学抗氧化剂研究的合著者是药理学和毒理学助理教授亚当·史密斯;史密斯实验室的研究生凯尔·戈斯曼和本杰明·戴克斯特拉;以及德尔·尚克尔结构生物学中心蛋白质生产组主任菲利普·高。
在一系列的测试中,堪萨斯大学的研究人员评估了注射小鼠的记忆与没有注射玉米蛋氨酸亚砜的类似小鼠的记忆。
Moskovitz说:“我们通过一个‘Y’迷宫来测量短期记忆能力,这对阿尔茨海默氏症非常重要,因为当人们患上阿尔茨海默氏症时,他们的短期记忆正在消失,而旧的记忆仍然存在。”“你把一只老鼠放在一个‘Y’形的迷宫里,这样它们就可以用左臂或右臂。但是当你把第三只手臂放在中间,如果他们认出第三只手臂是新的,他们会花更多的时间探索新手臂,因为他们有好奇心。如果他们甚至没有注意到还有第三只手臂——因为他们在看到它的那一刻就忘记了——他们会花更多的时间在右臂或左臂上。”
根据莫斯科维茨的说法,与对照组相比,注射了富含蛋氨酸亚砜(MetO)蛋白质的小鼠的记忆力大约提高了50%。
在另一个实验中,老鼠被要求在水迷宫中找到一个平台。
“我们给了它们六天的学习时间,即使是那些患有阿尔茨海默氏症的老鼠最终也学会了平台的位置,但我们发现第二天之后就有了很大的不同,注射了抗原的老鼠比未接种疫苗的老鼠学习得快得多,”莫斯科维茨说。“然后我们移走平台,看看他们是否仅凭记忆,而不是通过观察来记住平台的位置。我们再次看到了很大的不同。与未接种抗原的对照组小鼠相比,接种了抗原的小鼠能记住并在训练平台附近停留更多时间。”
除了短期记忆研究表明,改进后的抗原注入老鼠表现出更好的长记忆能力,血浆和大脑中的β -淀粉样蛋白水平降低,以及“减少β-淀粉样蛋白海马和皮质区星形胶质细胞的负荷和MetO积累;激活的小胶质细胞水平降低;以及在同一大脑区域提高抗氧化能力(通过增强转录因子Nrf2的核定位)。”
研究人员发现,研究中收集的数据很可能是转化性的,这表明主动免疫“有可能延迟或预防AD的发生”。
莫斯科维茨说,随着老年痴呆症风险的增加,可以对人们进行这种免疫接种,“大约在人们五六十岁时被告知第一次去做结肠镜检查,”他说。“进一步的加强注射可以维持免疫,这是人们从COVID疫苗中非常熟悉的一个过程。”
主动免疫是对目前被动免疫制度的改进,因为蛋氨酸亚砜抗原刺激免疫系统产生自身抗体。在被动免疫中,抗体直接注射到体内,但可能有严重的毒副作用(如脑炎),以及容易被免疫排斥免疫系统随着时间的推移成为非自身抗体。
Moskovitz说,这方面研究的下一步将是进行临床前和临床前研究临床试验与感兴趣的制药公司共同赞助。
进一步探索