2022年3月24日功能
CAR - T细胞免疫治疗实体瘤?首先,你必须打破癌症的糖盾
CAR - T细胞疗法是一种突破性的方法,在实验室中对患者的T细胞进行增压,重新注入后攻击癌症,对血液癌症的治疗比实体肿瘤更有效。
现在,一项新的研究旨在找出为什么以及如何克服这一问题实体肿瘤最近,意大利米兰的科学家们发现,实体肿瘤用一层糖衣保护自己,使它们能够抵抗CAR - T细胞的攻击。IRCCS San Raffaele科学研究所创新免疫疗法部门的Beatrice Greco及其同事正在探索克服它的方法。他们正在设计一种分子鱼雷,可以打破糖盾,从而为CAR - T细胞清除路径,并摧毁实体癌症。
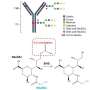
CAR - T细胞——嵌合抗原受体T细胞——最初是从患者血液样本中分离出来的T细胞。接下来,这些细胞在实验室中使用基因修饰过程进行修饰,使T细胞在其表面表达一种寻找并摧毁癌症的受体。
尽管进行了多年的研究,医学科学家们仍无法诱导增压T细胞像治疗恶性血液病那样有效地对抗实体肿瘤。癌细胞表面的糖基化,即癌细胞在一层厚厚的糖分子外衣中强化自身的过程,导致了使用CAR - T治疗各种实体肿瘤的困难。
涉及动物模型的实验室研究表明,糖问题的解决方案可能会进入人体临床试验在不远的将来。
“嵌合抗原受体工程T细胞的免疫治疗在难治性B细胞恶性肿瘤患者中表现出了非凡的成功,”Greco在报告中写道科学转化医学。“然而,先进-人类研究在实体瘤中发现了独特的障碍,导致疗效证明不佳。理解CAR - T细胞识别肿瘤的决定因素应该转化为能够克服耐药性的策略设计。”
阻碍CAR - T细胞疗法在实体肿瘤中发挥作用的不仅仅是糖的问题,尽管碳水化合物涂层一直是成功治疗的最大障碍。实体肿瘤的微环境有助于防止CAR - T细胞正常浸润肿瘤部位。此外,实体瘤也很少有CAR - T细胞可以轻易识别和锁定的抗原。
米兰的科学家说,世界各地的研究人员都在研究如何克服这些障碍,但还需要做更多的工作来了解影响CAR - T细胞能否识别其恶性靶细胞并与其相互作用的因素。
为了了解为什么几乎每种类型的实体肿瘤都对CAR - T细胞疗法有耐药性,Greco和同事们在细胞保护自己免受破坏方面寻找这些癌症的共同点。研究小组发现,“多种癌症表达细胞外n聚糖,其丰度与CAR - T细胞杀伤呈负相关。”
n链糖基化是指一个关键的化学过程,在这个过程中,寡糖转移酶(一种酶)催化寡糖转移到氨基酸受体上,在这种情况下是天冬酰胺。低聚糖是由一串单糖亚基组成的碳水化合物。
把它想象成一个过程,一个由多个单元组成的链条,一次又一次地连接在一起的过程。每次寡糖附着在暴露的天冬酰胺上,都是链上的另一个环节。最终的结果是糖分子的紧密链在癌细胞上建立了一个堡垒。在宏观层面上,肿瘤被糖保护,使癌症免受攻击。Greco和他的同事们说,n链糖基化是实体肿瘤抵抗CAR - T细胞免疫疗法的关键。
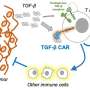
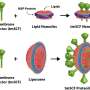
Greco和同事发现,在CAR - T细胞中加入糖类似物(一种起到鱼雷作用的抗糖分子),可以增强被栓塞的T细胞的杀伤能力。由于癌细胞有多种方法来逃避任何形式的治疗,她和她的团队说,将抗糖分子结合到CAR - T细胞治疗中,可以帮助克服肿瘤可能用来保护自己的多种伎俩。
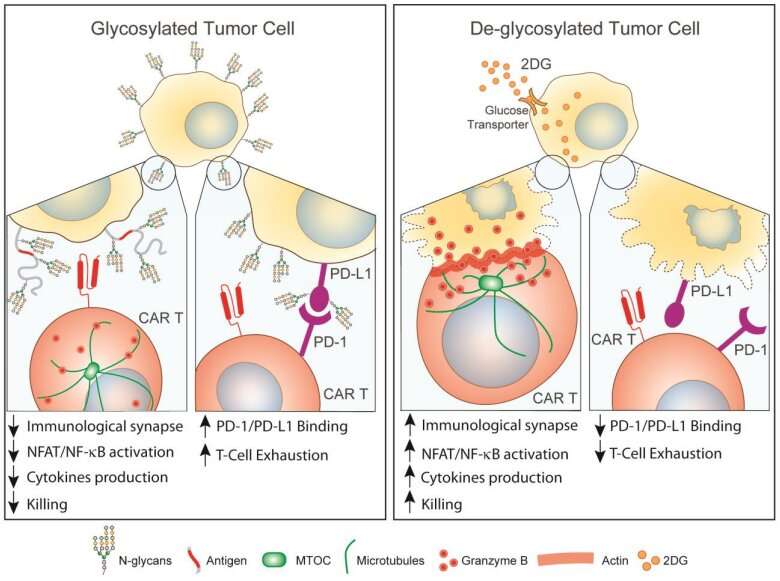
“我们发现n -聚糖通过干扰适当的免疫突触形成和减少转录激活、细胞因子产生和细胞毒性来保护肿瘤免受CAR - T细胞的杀伤,”Greco写道。“为了克服这一障碍,我们利用肿瘤的高代谢需求来安全抑制n -聚糖的合成。”
胰腺细胞在其表面大量的碳水化合物- n -甘聚糖中保护自己。n -聚糖在胰腺癌中作为对抗CAR - T细胞的力场。恶性肿瘤是最难治疗的癌症之一。能够使用CAR - T细胞免疫疗法可能会增加医生将来可能依赖的医疗设备。
为了解决糖衣问题,研究小组使用了一种分子鱼雷——2-脱氧-d -葡萄糖——一种可以抑制n -聚糖合成的糖类似物。研究人员发现,用2-脱氧-d -葡萄糖治疗小鼠胰腺肿瘤会破坏肿瘤细胞的n -聚糖屏蔽层,使它们更容易受到CAR - T细胞治疗的影响。
此外,联合治疗(2-脱氧葡萄糖+ CAR - T细胞免疫治疗)也使一系列其他实体肿瘤对CAR - T细胞治疗敏感。这些实体肿瘤包括肺癌、卵巢癌和膀胱癌。
虽然米兰和其他地方的研究人员正在研究如何克服阻碍CAR - T细胞摧毁癌症的障碍,但还需要做更多的工作来了解影响CAR - T细胞能否识别恶性靶细胞并与其相互作用的因素。
即使是在血液病癌症中,最近一系列研究估计,CAR - T细胞疗法只有30-40%的成功率才能持久缓解。这意味着相当多的患者并没有从治疗的承诺中受益。
为了提高成功率,世界各地实验室的医学科学家正在寻找制造CAR - T细胞的方法癌症治疗对血液癌和实体癌都更有效。
“总的来说,我们的研究结果表明肿瘤n -糖基化调节CAR - T细胞反应的质量和大小,为改进实体恶性肿瘤治疗的合理设计铺平了道路,”Greco说。
进一步探索
©2022科学BOB体育赌博X网络