一个错误的识别案例:研究人员揭开了巴雷特食管的细胞来源
对于身体内的大多数细胞来说,身份是不容置疑的。膀胱细胞不能模仿血细胞。肝细胞仍然是肝细胞。
其中一个罕见的例外被认为是巴雷特病食道在这种情况下,食道的内壁与小肠的内壁很相似。虽然它本身无害,但却是食道腺癌发展的最大危险因素癌症在食道和胃.
达纳-法伯癌症研究所的科学家们最近进行的两项研究纠正了长期以来关于巴雷特食道起源的误解,并由此指出了降低食管癌风险的治疗或预防新途径。第一项研究去年发表在该杂志上胃肠病学,证明巴雷特食管实际上并不涉及食管细胞变成肠细胞但胃细胞具有肠细胞的一些特征。第二项研究发表在最新一期的基因与发育,追踪了一系列分子事件的发生。
“巴雷特食管是由长期胃肠反流疾病(GERD)引起的,胃酸反复流回食管,”丹娜-法伯和布里格姆妇女医院的Ramesh Shivdasani医学博士说,他是这两篇论文的资深作者。“接触胃里的酸性物质会导致胃和食道交界处的细胞发生变化。在胃肠化生(GIM)中也可以看到非常相似的变化,这种疾病发生在胃的下部。”
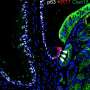
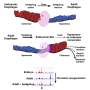
这些变化在显微镜下很容易看到。消化道的内壁是由上皮细胞组成的。在食道中,它们以鳞状或分层细胞的形式出现,这些细胞水平分层,就像墙上的砖一样。在肠道中,它们被称为柱状细胞,类似于垂直堆叠的砖块。分层细胞具有保护功能,防止有害物质与下层细胞接触;柱状细胞从食物中吸收营养。在患有巴雷特食管的患者中,食管和胃交界处的细胞本应呈分层状,但看起来却完全像柱状的肠细胞。
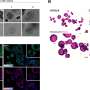
在胃肠病学在论文中,Shivdasani和他的同事们在分子水平上研究了这些看似肠道的细胞。他们专注于细胞的染色质——它们的DNA和蛋白质包裹。染色质的结构就像一根绕在多个线轴上的纱线:DNA紧紧地缠绕在一起,基因是沉默的;在松弛的地方,基因是活跃的。细胞内DNA盘绕和展开的模式表明了细胞的核心身份,即它在体内的基本作用。每种类型的细胞,无论是大脑、骨骼还是神经细胞,都有独特的染色质特征。
Shivdasani和他的同事检查了人类巴雷特食管组织活检样本中的染色质组织。他说:“当我们分析整个样本时,每个样本都包含数千或数万个细胞,我们发现了胃细胞和肠细胞的非常明确的特征。”“但没有食管的痕迹。”
这一发现也留下了相当大的模糊:这些组织是由胃和肠细胞的混合物组成的,还是由部分胃和部分肠性质的细胞组成的?
当技术的进步使研究人员能够探测单细胞内的染色质组织时,答案就来了。该团队的分析表明,巴雷特食管细胞“本质上是一种精神分裂症或混合细胞,具有胃和肠道的特征,”Shivdasani评论道。“这告诉我们巴雷特食道和GIM的核心是什么。”
这一发现表明,巴雷特食管并没有违反一种细胞类型完全转变为另一种细胞类型的信条。但它留下了一个悬而未决的问题,即胃细胞如何具有某些肠细胞的特性。
的基因与发育论文是解决这一难题的重要一步。这一步涉及到一种名为HNF4A的转录因子——一种控制基因活性的蛋白质,它通常存在于胃细胞中,含量较低。Dana-Farber的Harshabad Singh医学博士发现,高水平的HNF4A激活了第二种叫做CDX2的因子,这种因子在正常的胃细胞中永远不会产生,但却需要激活肠道基因。
Singh是这两项研究的第一作者,他继续表明CDX2可以开启大约四分之一的肠道相关基因。希夫达萨尼说,尽管这项研究主要是在小鼠组织中进行的,但它可能也适用于人类组织。
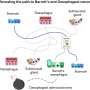
这些发现使研究人员能够构建一个关于巴雷特食管发育过程中在细胞和分子水平上发生了什么的假设。希夫达萨尼解释说:“巴雷特氏食道及其引起的癌症在少数情况下总是发生在食道的最底部,在那里正常的分层上皮与胃的柱状上皮相遇。”“我们的理论是,食管内膜的一些损伤——比如慢性胃酸反流引起的损伤——太严重了,以至于食管上皮细胞无法自行愈合。受损区域需要某种屏障,所以胃上皮细胞会移动到那里来封闭缺口。当他们到达时,他们就会留下来胃癌细胞但局部环境触发了诱导肠道特性的转录因子。”
他继续说,这项研究最终可能会产生预防或缓解巴雷特食道的治疗方法。“要治疗这种性质的疾病,有必要确切了解涉及的细胞类型。知道了巴雷特食管的真实身份细胞而它们的分子触发因素是重要的第一步。”
Harshabad Singh等,转录因子介导的肠化生和阴影增强剂的作用,基因与发育(2021)。DOI: 10.1101 / gad.348983.121