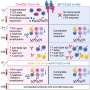
欧盟授权该公司第五COVID疫苗
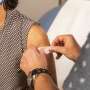
周一欧盟委员会(European Commission)批准疫苗从我们公司该公司作为其第五在欧盟官方注射使用,小时后欧盟药品监管机构批准。
官员希望疫苗,由比其他人更传统的技术,将有助于说服那些犹豫是否接种疫苗。
“一次ο变体迅速蔓延,而我们需要加强疫苗接种和政府的支持者,我特别满意今天的授权该公司疫苗,”欧盟首席乌尔苏拉•冯德莱恩说。
诺瓦瓦克斯公司疫苗现在坐落与欧盟的其他授权COVID刺痛,从BioNTech /辉瑞、现代化、阿斯利康和强生(Johnson & Johnson)。
称为Nuvaxovid,诺瓦瓦克斯公司提供疫苗是基于所谓的蛋白质亚基技术尝试和测试,已经使用了几十年接种人对抗疾病,包括乙型肝炎和百日咳。
与信使核糖核酸疫苗由BioNTech /辉瑞和现代化,Nuvaxovid不需要存储在极低的温度,使它难以介入物流优势地区。
的有前景的结果
周一早些时候,欧洲药品局(EMA)开了绿灯的注射给予有条件的市场营销授权。
仔细研究的临床数据从英国和在美国和墨西哥的研究已经显示“健壮”,满足欧盟标准“有效性、安全性和质量”,它说。
冯德莱恩在她的声明中说,她希望最新的除了欧盟范围的疫苗会”提供一个强有力的鼓励每个人尚未接种疫苗或提高了,现在是时候这样做”。
欧盟卫生专员Stella Kyriakides说Nuvaxovid“反COVID-19显示了有前景的结果”。接种疫苗和支持者是“今天比以往任何时候都更重要的是如果我们要阻止感染和计数器的波的出现和传播新变体”,她说。
美国一家生物技术公司总部位于马里兰州,已经获得应急使用批准的疫苗在印尼和菲律宾,和日本已同意购买1.5亿剂。
它还将向美国监管机构提出申请,美国食品和药物管理局,说,该公司的生产和vaccine-vetting过程已经饱受延误。
该公司表示,它还在英国申请批准,印度、澳大利亚、新西兰、加拿大、和与世界卫生组织(世卫组织)。
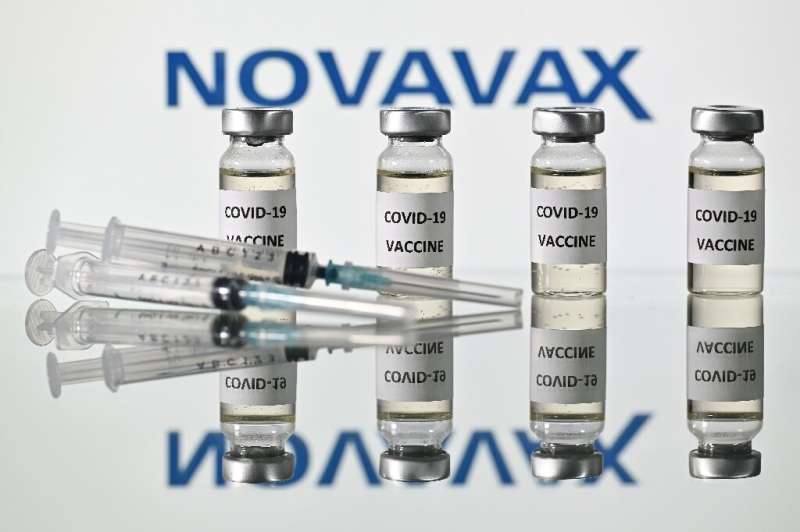
“数据有限”的买卖
该公司首席执行官斯坦利Erck表示,欧盟委员会的授权将疫苗”在关键时刻当我们相信选择疫苗会导致增加免疫”。
疫苗”可以帮助解决全球疫苗接种的主要障碍,包括全球分销的挑战和疫苗犹豫”,Erck补充道。
EMA指出,虽然Nuvaxovid的两个主要临床试验显示,在89 - 90之间疗效减少COVID症状的情况下,这是对α和β的COVID变异不再流行。
“目前有限的疗效数据Nuvaxovid对其他变异的担忧,包括买卖,”它说。
捐赠的剂量
从表面上看,欧盟并不需要另一种疫苗。
它有69%的人口充分接种疫苗,并已获得预先购买42亿剂从七疫苗制造商。
很大程度上是依靠BioNTech /辉瑞,占超过一半的疫苗已经购买或选择。
但欧盟也是世界上最大的出口国的疫苗,包括剂量时从工厂发送集团合同,别人给了世卫组织领导的Covax设施,和其他捐款。
即使Nuvaxovid看到欧盟有限使用,它可以加强供应欧盟成员国已经承诺发送到世界的其他地方。
欧盟签署了其预购协议,该公司今年8月,批准和授权。这笔交易将看到美国公司提供1亿剂从明年年初开始,和一个额外的1亿到2023的选项。
成员国已经锁定在2700万份订单。
©2021法新社