新的web服务器有助于识别COVID-19候选药物
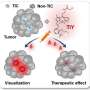
莱斯大学的研究人员推出了一个在线门户网站,帮助研究人员筛选可能攻击SARS-CoV-2病毒特定蛋白质的COVID-19候选药物。
George R. Brown工程学院的计算机科学家Lydia Kavraki和她在休斯顿大学、苏格兰爱丁堡大学和巴西Ceará联邦大学的同事们发布了一个“用户友好”的网络服务器,为科学家们提供了筛选他们的研究成果的机会候选药物实际上与SARS-CoV-2病毒上已知的蛋白质结合袋有关。
更好的是,该程序还包含了他们所说的在这些口袋的计算模型中经常被忽视的一个因素:它们的灵活性。
该项目在一篇开放获取的论文中详细描述生物与医学中的计算机,结合了三种药物靶点-主要蛋白酶(Mpro)、RNA依赖RNA聚合酶(RdRp)和木瓜蛋白酶样蛋白酶(PLpro)模型,通过DINC-COVID进行集成对接。
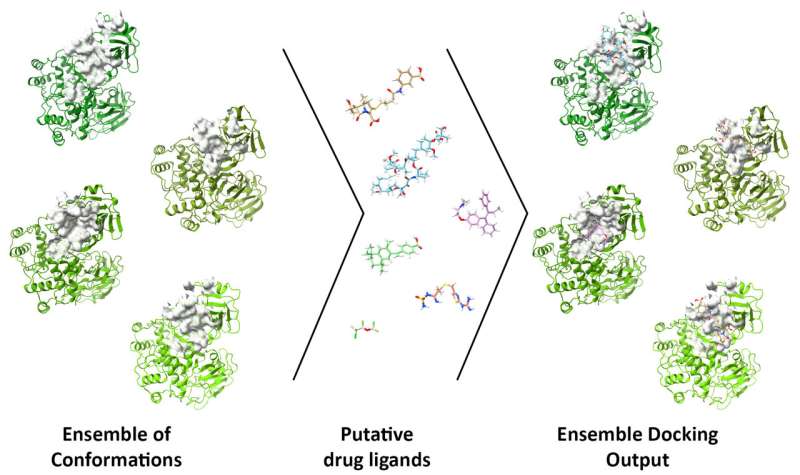
集成对接方法允许研究人员针对SARS-CoV-2蛋白的不同构象及其结合袋筛选候选配体(反应分子)。然后,DINC-COVID对配体的成功结合进行评分。
DINC代表“增量对接”,这是卡夫拉基实验室在2013年开发的一种协议,旨在加快蛋白质-肽对接模拟,帮助研究人员设计药物、疫苗和其他涉及大配体的过程。卡夫拉基和当时她实验室的博士后研究员、现在休斯顿大学的助理教授迪勒·安图内斯(Dinler Antunes)领导的升级版于2017年出现。
新的迭代依赖于迄今已解决的SARS-CoV-2蛋白质结构的“令人印象深刻的数量”。了解这些结构可以让研究人员找到理想的结合伴侣,从而使病毒失活。
这项研究还提供了一个字面上的扭曲,最能体现这一点的是main蛋白酶在过去18个月里,该网站一直是人们关注的焦点。研究人员发现,Mpro位点可以在结合过程中极大地扭曲其形状,使其能够适应各种各样的潜力配体.
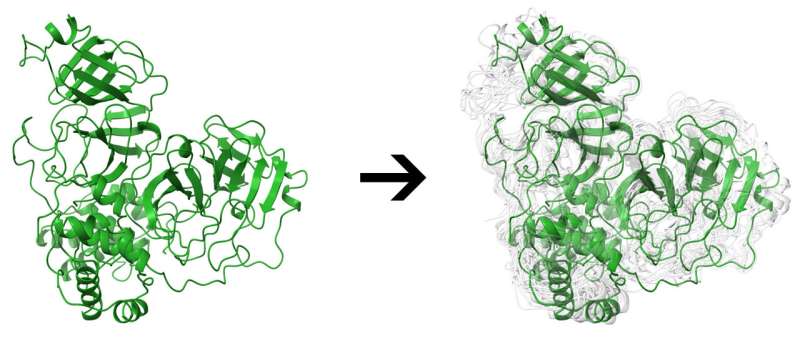
赖斯大学博士后研究员、合著者毛里西奥·里戈(Mauricio Rigo)说,这种可塑性使得Mpro和其他网站难以模拟,计算成本要高得多。“与其他服务器不同,我们提供的蛋白质不是静态的;它们不是单一的构象,”他说。“我们使用状态来反映这种蛋白质在生理环境中的动态。”
例如,该团队使用几个程序将由分子动力学模拟生成的10万个可能构象缩小到一组具有代表性的构象。这使得研究人员可以将集成生成与DINC-COVID内的对接分离,从而在复杂的计算上节省数小时或数天。
“我们相信这是正确的做法,”里戈说。“我们对算法的测试与实验结果吻合得很好。”
与Mpro一起,该团队模拟了PLpro和RdRp上催化结合位点的集合。对于Mpro,他们模拟了它的催化和变构结合位点,总共有12个集合。
“我们选择它们是因为它们可以被不同的药物靶向,”莱斯大学研究生、该论文的联合主要作者萨拉·霍尔-斯旺说。“当你试图找到一种药物来抑制病毒时,你会寻找它蛋白质那些对病毒发挥作用很重要的部分,并试图抑制它们。”
该实验室正在努力扩大DINC-COVID中可用的集成数量。
“我们对社区对我们工作的反应非常满意,”卡夫拉基说。“DINC- covid已经被16个不同国家的约500名研究人员使用,而我们早期的网络服务器DINC已被1.1万名用户访问。我们希望DINC-COVID将有助于阐明SARS-CoV-2感染的复杂机制。”
Didier Devaurs是前莱斯大学博士后研究员,现在是爱丁堡大学的研究员,他是这篇论文的共同第一作者。Geancarlo Zanatta, Ceará联邦大学物理学副教授,通讯作者。Kavraki是诺亚哈丁计算机科学教授,生物工程、机械工程、电气和计算机工程教授,肯肯尼迪研究所所长。
更多信息:Sarah Hall-Swan等人,DINC-COVID:与灵活的SARS-CoV-2蛋白集成对接的网络服务器,生物与医学中的计算机(2021)。DOI: 10.1016 / j.compbiomed.2021.104943