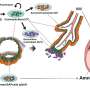
科学家们确定了一个基因在胎盘发育中的重要作用
国家心血管研究中心(CNIC)的科学家利用实验小鼠模型确定了GPR126基因在怀孕期间胎盘发育中的重要作用。
研究结果发表在科学的进步,表明GPR126(黏附G蛋白偶联受体126)对前列腺癌有重要作用发展一种特殊的胎盘细胞类型,调节子宫血管的重塑。小鼠Gpr126突变体的心脏缺陷继发于胎盘缺陷,反映了胎盘和胎盘之间的密切关系胎儿心脏.
有证据表明,GPR126可能在人类胎盘发育中发挥类似的作用。携带GPR126突变基因的女性的婴儿会在妊娠期间或出生后不久死亡,其中30%的女性会患上先兆子痫。这种妊娠并发症在一般人群中影响5 - 8%的妊娠,其特征是高血压这会损害母亲和胎儿,并可能导致胎儿死亡。
动物模型实验表明,GPR126对于周围神经系统(PNS)的成熟、骨骼和软骨的形成以及内耳的发育都是必需的。在人类中,GPR126的突变与骨骼畸形和四肢肌肉痉挛有关。
由José Luis de la Pompa博士领导的CNIC细胞间信号在心血管发育和疾病组,最初确定GPR126是在研究过程中受NOTCH信号通路(动物中高度保守的细胞间信号系统)调控的基因心发展。
这表明GPR126可能影响发育中的心脏心肌细胞(心肌细胞)的增殖和分化。
其他研究小组已经提出在小鼠和斑马鱼的心脏发育中需要GPR126,但研究还没有提供确凿的证据来证实这一假设。
这项新研究发表在科学的进步在美国,CNIC团队使用遗传技术证明,GPR126不是小鼠心脏发育所必需的,但在胎盘形成(称为胎盘形成)中起着重要作用。
在解释研究结果时,德拉庞帕博士说:“我们观察到,小鼠体内GPR126的全身失活导致心壁变薄,并导致胚胎死亡。然而,当我们在心脏中灭活该基因时,胚胎发育不受影响,心脏功能也没有改变。”
研究人员还发现,全身GPR126缺失的致命作用“并没有通过GPR126在心脏中的特异性重新表达而逆转,这表明突变体的胚胎死亡并不是由于心脏发育缺陷造成的,”第一作者Rebeca Torregrosa解释道。
对斑马鱼模型的进一步研究证实,GPR126“与心脏发育无关”。
胚胎发育
在胚胎发育期间,GPR126在巨型滋养细胞中表达,这是一种胎盘特有的细胞类型。“这些细胞,”de la Pompa指出,“对于胚胎着床和维持妊娠至关重要。”
研究小组证明,如果胎盘保留至少一个正常的GPR126基因拷贝,胚胎中的GPR126失活与存活是兼容的。然而,胚胎和胎盘中该基因的失活会导致胚胎死亡。
“胎盘发育的关键步骤之一是母体动脉的重塑。这些血管被称为螺旋动脉,它们增加了直径,以增加流向胚胎的血液。这一过程中的缺陷与妊娠并发症有关,如子痫前期、胎儿生长受限,甚至流产,”José Luis de la Pompa说。
研究表明,滋养层GPR126对于参与螺旋动脉重塑的特定蛋白酶的表达是必要的,而螺旋动脉重塑对胎儿的生存能力至关重要。
基于这些结果,研究人员宣布缺乏GPR126的小鼠可作为研究螺旋动脉重塑和子痫前期的实验模型。这动物模型在胚胎植入前遗传学诊断中具有潜在的临床应用价值。
进一步探索