为什么短期肺部感染会导致长期肺部损伤?
病毒性呼吸道疾病中最致命的时刻有时实际上是病毒从体内清除之后。在病毒被击败后的几周内,在感染高峰期间启动的破坏过程会导致器官损伤,从而导致慢性疾病甚至死亡。例如,在第一次COVID-19发作后,一些人会持续咳嗽、呼吸困难和呼吸短促,这些都是持续肺部疾病的症状。
圣路易斯华盛顿大学医学院的研究人员已经找到了线索肺呼吸衰竭后会出现损伤感染.通过对小鼠的研究,他们发现感染会引发一种名为IL-33的蛋白质的表达,这种蛋白质是人体所需的干细胞在肺中过度生长进入空气空间,并增加粘液的产生和肺部炎症。该研究结果发表在8月24日的《美国医学杂志》上临床研究杂志,揭示预防慢性肺损伤的潜在干预点病毒感染.
资深作者、塞尔玛和赫尔曼塞尔丁医学教授、细胞生物学和生理学教授迈克尔·j·霍尔茨曼医学博士说:“疫苗、抗病毒药物、抗体疗法都是有帮助的,但对于已经处于进步性疾病之路的人来说,它们不是解决方案。”“我们在照顾COVID-19引起的急性疾病方面做得更好,但初始损伤阶段之后发生的事情仍然是取得更好结果的主要障碍。在这一点上,我们还面临着数千万已经感染的人,其中很大一部分人患有长期疾病,特别是呼吸道症状。我们没有一种治疗方法可以纠正这个问题。”
人们早就认识到急性呼吸道感染可导致慢性肺部疾病。例如,感染呼吸道合胞病毒住院的儿童患哮喘的可能性是普通儿童的两到四倍,哮喘可能持续很长一段时间,甚至可能持续一生。然而,急性呼吸道感染究竟是如何引发慢性疾病的尚不完全清楚,因此很难开发出预防或治疗它的疗法。
作为这项研究的一部分,Holtzman和他的同事,包括第一作者、医学讲师吴康云博士,研究了感染仙台病毒的小鼠。仙台病毒不会对人类造成严重的疾病,但它会自然地感染包括老鼠在内的其他动物,并引起呼吸道感染,其发展很像人类的呼吸道感染。
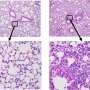
研究人员检查了感染仙台病毒12天和21天后小鼠的肺组织,并将样本与未感染小鼠的肺组织进行了比较。他们发现,在未感染的小鼠体内,两种干细胞有助于维持肺与外界之间的屏障。然而,在感染仙台病毒后,这两个种群分别开始繁殖并扩散到空气中。基底细胞接管小气道和气囊,而AT2细胞仍然局限于气囊。一些新的基底细胞成为粘液生成细胞,而另一些则释放分子,将免疫细胞招募到肺部。总的来说,这个过程会导致肺部的空气空间减少,粘液增多,持续的炎症影响呼吸。
进一步的实验表明,这一过程取决于蛋白质IL-33。在正常情况下,IL-33在肺干细胞核中增加,以应对压力或损伤,并帮助肺修复受损屏障。然而,在感染期间和感染后,IL-33可以发挥更有害的作用。
目的探讨IL-33在病毒后的作用肺损伤研究人员对小鼠进行了基因改造,使其在肺干细胞的基础组中缺乏IL-33。然后,科学家们用仙台病毒感染了这些小鼠——以及另一组未经过基因改造的小鼠。两组小鼠在抵抗最初的仙台病毒感染方面同样有效。但在感染三周后,缺乏IL-33的小鼠的肺部表现出更少的细胞过度生长、粘液和炎症,这表明它们的肺部有害变化的迹象更少。在感染后7周,基底细胞中没有IL-33的小鼠血液中的氧含量也更高,气道高反应性也更低,这两者都是慢性肺部疾病改善的迹象。
霍尔茨曼说:“这些结果真的很令人高兴,因为去除IL-33,反过来失去基础干细胞可能会使情况变得更糟。”“转基因小鼠可能已经死亡,因为它们不再能够正常修复病毒对肺屏障的损伤。但事实并非如此。的老鼠缺少这样的人口基底细胞结果反而好得多。这正是我们感到兴奋的地方。这些发现为我们找到纠正基底茎不良行为的疗法提供了坚实的基础细胞."
Holtzman说,针对IL-33和基底细胞激活之间通路的步骤,可以形成广泛有效的治疗方法的基础,以预防或治疗由各种病毒引起的肺部疾病,也可能是肺部和身体与外界接触的其他部位的其他形式的损伤。
霍尔茨曼说:“肺对损伤有相当刻板的反应,包括病毒损伤。”“特定类型的病毒、宿主的基因、最初疾病的严重程度——所有这些都会影响结果,但它们只是程度的问题。你仍然可以在各种情况下看到相同的关键因素,这就是为什么我们相信可以有一个共同的治疗策略。我们有一个药物发现计划来寻找这样一种常见的策略,而这项研究很符合这一点。”
进一步探索