研究揭示了婴儿癫痫发作的潜在原因

研究人员报告说,婴儿痉挛是一种罕见但严重的婴儿癫痫发作障碍,似乎是分子通路出错的结果。在他们对这种疾病的小鼠模型的研究中,研究人员发现,与这种疾病相关的基因突变损害了在海马体中建立新突触的通路,海马体是学习和记忆所必需的大脑区域。
该研究结果发表在期刊上EMBO报告,还详细介绍了潜在的治疗干预措施的使用,以解决一些经常与之相关的发育问题婴儿痉挛症.
伊利诺伊大学香槟分校分子和综合生理学教授蔡念培说:“我们正在试图了解婴儿痉挛患者学习和记忆障碍背后的原因。”蔡念培和伊利诺伊大学的研究科学家李关荣一起领导了这项研究。蔡崇信是伊利诺伊大学贝克曼高级科学与技术研究所的教员。
蔡崇信说,虽然婴儿痉挛通常在四五岁时消失,但影响记忆和学习的长期发育问题仍然存在。
他说:“学习和记忆障碍是长期的,患者在学校经常需要帮助。”“这告诉我们,癫痫发作和学习缺陷可能是由大脑中的不同问题引起的,但没有人真正知道是怎么回事。”
Tsai说,先前的研究发现,婴儿痉挛通常与一种名为Nedd4-2的基因突变有关,这种基因编码一种称为连接酶的蛋白质,调节神经元的兴奋性。
他说:“为了研究这种基因的作用,我们使用了Nedd4-2从大脑中选择性去除的小鼠作为模型,以模拟Nedd4-2受损的患者。”
研究人员对Nedd4-2连接酶功能受损的小鼠和功能正常的小鼠进行了行为和生理实验。他们还研究了缺乏连接酶如何影响在细胞培养中生长的小鼠神经元的生化途径。
他们发现,海马体中缺乏足够Nedd4-2连接酶水平的雄性小鼠学习和记忆能力受损。这种残疾与兴奋性结构的问题有关突触海马区负责在神经元之间传递电信号。研究人员关注海马体中的神经元,因为这个大脑区域在将短期记忆转化为长期记忆方面起着关键作用。
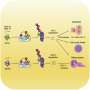
他们的实验表明,海马体中缺乏Nedd4-2破坏了一种调节微丝生长的途径,这种微丝被称为肌动蛋白,支持突触等细胞结构的形成。缺乏足够水平的连接酶的细胞经历了这些细丝的破坏,并在海马体中有较少的兴奋性突触。
“突触需要结构支持来维持其功能和完整性,”Tsai说。“肌动蛋白是细胞中的关键结构成分之一,由单体组成,它们可以相互附着形成聚合物。当肌动蛋白聚合物在突触中形成时,突触变得更强。这一过程对学习和记忆至关重要。”
当研究小组将缺乏足够Nedd4-2水平的小鼠暴露于一种模仿Nedd4-2活性的药物化合物中连接酶在大脑中老鼠似乎恢复了一些失去的依赖海马体的记忆。研究人员发现,同样的化合物在细胞培养中恢复了海马兴奋性神经元。
“因为我们证明了一些与婴儿痉挛相关的学习和记忆问题可以通过动物合成肽来改善,这意味着有一天我们可能能够从医学上增强学习和记忆能力内存携带这种Nedd4-2基因突变的患者,”Tsai说。
更多信息:Lee Kwan Young等人,婴儿痉挛‐相关Nedd4‐2通过科非林信号调节海马可塑性和学习,EMBO报告(2021)。DOI: 10.15252 / embr.202152645