分子桥介导皮层抑制性突触特异性
金门大桥以其令人惊叹的景色和惊人的身材,当之无愧地成为现代世界奇迹之一。它优雅的装饰艺术风格和标志性的塔楼为游客提供了一生一次的震撼照片的机会。金门绵延近2英里,是一个重要的门户,促进了思想、商品和人员的交流。
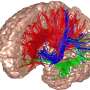
虽然没有这么大的规模,但我们的大脑有类似的连接神经元的通道。这些被称为突触的小隔间,使信息的动态交换和神经回路的形成成为可能。为了构建这些回路,发育中的神经元必须首先遵循特定的引导线索,在大脑中传播,直到找到合适的伙伴。这个过程在很大程度上是重要的大脑皮层它由六个功能和解剖学上不同的层组成。尽管人们对皮层进行了广泛的研究,但对于皮层内驱动突触特异性的精确分子机制却知之甚少。这对于一种叫做抑制性中间神经元(INs),通常只使用一层或两层进行本地连接。揭示起作用的分子将进一步理解皮层抑制回路的形成。
在最近的一篇杂志上科学的进步佛罗里达的谷口实验室已经阐明了皮层中抑制突触特异性的新机制。MPFI的科学家们发现了细胞粘附分子IgSF11的新作用,该蛋白介导了皮层吊灯细胞(ChCs)中的层特异性突触靶向。
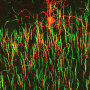
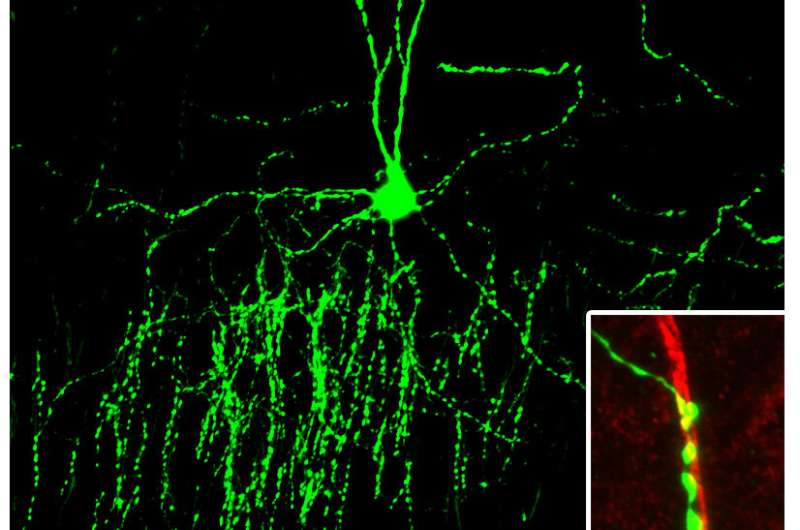
“我们的实验室专门研究皮层中间神经元和抑制回路的形成,”佛罗里达马克斯·普朗克研究小组负责人Hiroki Taniguchi博士描述道。“枝形细胞是我们最喜欢的中间神经元亚型之一,已被证明表达独特的遗传标记,只支配皮层内的某些层。(ChCs在皮层主要神经元中关键控制刺突的产生,并与精神分裂症和癫痫等脑疾病的病理有关。)我们认为,这种模型细胞类型将是我们开始寻找具有层特异性突触匹配的分子的完美地方。”
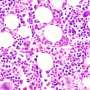
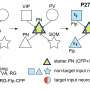
MPFI的科学家们开始了他们的研究,使用单细胞RNA测序从基因上筛选INs,以寻找单个亚型的独特基因。他们在一个有趣的类别中发现了一组基因细胞粘附分子,或CAMs。与其他in亚型相比,其中一种CAM IgSF11在ChCs中高度富集。

“我们对INs的基因筛选是我们第一次发现IgSF11的地方,”该出版物的第一作者、Taniguchi实验室的研究科学家Yasufumi Hayano博士解释说。“我们正在寻找编码细胞表面蛋白质的亚型特异性基因,认为那些在神经元外部表达的基因将是介导突触特异性相互作用的完美候选者。”
cam由一组不同的结构蛋白组成。CAMs通常被认为是一种生物胶水,在神经元的外部表达,并在大型复合物中相互作用,促进细胞间的相互作用。它们形成的桥状复合物为新形成的突触提供了稳定性,并有助于细胞粘附和交流。一类CAMs,称为嗜同性CAMs,只与与自己相同的其他CAMs相互作用,理论上有可能介导突触形成的特异性。
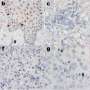
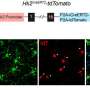
在确定IgSF11是一个亲质CAM后,MPFI团队在ChCs支配的皮层2/3层上半部分的神经元中寻找IgSF11的表达,推理出亲质CAM相互作用需要在两侧都发生表达。利用荧光原位杂交(FISH),研究人员发现IgSF11在ChC和位于皮层2/3层的靶神经元中均有稳定表达,但在其他层中没有,这为IgSF11相互作用在ChC突触特异性中起重要作用提供了强有力的证据。
接下来,Taniguchi实验室通过从大脑中去除IgSF11并检查变化,评估了IgSF11在ChC突触形成中的功能作用。为了分析IgSF11是只在ChCs上发挥功能,还是在ChCs和目标皮层神经元上都发挥功能,研究小组必须开发一种策略,允许选择性去除IgSF11。为了实现这一目标,MPFI的科学家们生成了IgSF11 KO小鼠,并将荧光鉴定的KO ChCs移植到野生型宿主动物中。KO ChCs表现出突触钮扣的大小和数量的显著减少。证实了IgSF11通过嗜同性相互作用赋予其特异性的假设,将wt ChCs移植到IgSF11 KO小鼠的大脑中也导致了同样的减少。综上所述,IgSF11似乎与ChC突触扣的发育和形态分化密切相关。
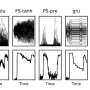
与MPFI的电子显微镜核心和Kwon实验室合作,进一步研究了KO IgSF11的功能后果。高倍电镜超微结构分析显示,KO ChCs中剩余的少数突触钮扣不能正常分化,并表现出突触传递的缺陷。支持这一数据的是,光遗传学辅助IgSF11 KO小鼠的电生理学表现出突触传递的额外缺陷。
“使用吊灯细胞的一个挑战是,它们很难用传统方法进行基因操作,”Hayano博士解释说。“为了克服这一问题,我们设计了一种新的基于病毒的策略,使用腺相关病毒将一种难以表达的蛋白质IgSF11传递到感兴趣的细胞。”
MPFI团队使用他们的AAV病毒策略来研究IgSF11在来自2/3层以外的不同皮层层的神经元中表达是否可以人工诱导与ChCs形成突触。他们用IgSF11转导V层神经元,发现这些细胞和枝形细胞之间形成了大量异位突触,这是在正常情况下不会发生的现象。
谷口博士指出:“IgSF11是第一个被发现的细胞粘附分子,它直接介导神经元间亚型,皮层中突触的层特异性形成。”“进一步阐明围绕抑制电路组装的分子机制,可能会在其他不同的中间神经元亚型中揭示类似的模式,并有助于揭示抑制电路是如何形成的。我们的工作可能为理解独特的中间神经元亚型电路缺陷引起的神经发育障碍的病因学提供了一个有用的切入点。”