在耐辐射胰腺癌细胞中找到弱点
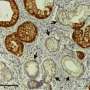
在已知的所有不同类型的癌症中,一种称为胰腺导管腺癌(PDAC)的胰腺癌亚型是最具侵略性和致命的癌症。该疾病始于胰腺中某些小管道的细胞,并静静地进展,通常不会引起症状,直到晚期肿瘤实际上阻碍了这些管道或扩散到其他地方。PDAC不仅很难诊断,而且对可用治疗的反应也不反应。特别是,研究人员指出,PDAC细胞通常可以通过在很大程度上未知的机制来生存放疗。
日本国家量子与放射科学技术和放射科学与技术研究所的放射与癌症生物学小组的一部分,日本Sumitaka Hasegawa博士和同事Motofumi Suzuki和Mayuka Anko目前正在研究使PDAC的原因细胞因此,耐辐射,如果有办法打破他们的防御能力。在他们的最新研究中,发表在国际辐射肿瘤学杂志,生物学,物理学,他们设法揭示了PDAC中抗药性之间的好奇关系的一些奥秘,细胞周期,以及一个称为的过程自噬- 或“自我消算”。
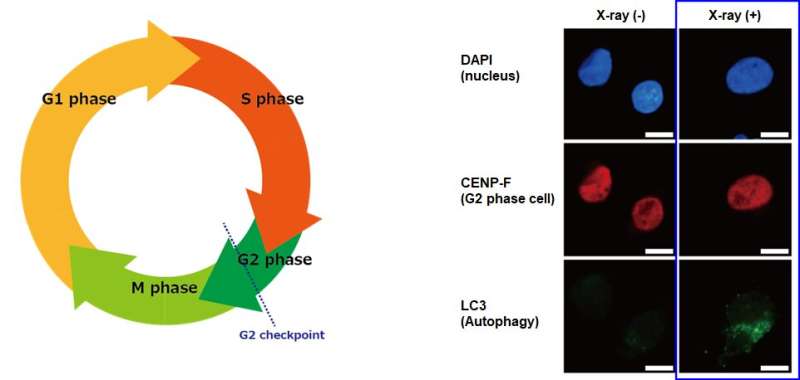
从一个细胞分裂到下一个细胞,我们体内的每个细胞都是完成无数细胞周期的结果。图1中示意性地显示的每个细胞周期都是一个化学策划的阶段序列,其中许多蛋白质会主动控制细胞的生长并确保其安全分裂。当遇到DNA损伤时,将细胞周期停止在所谓的G2检查点,并将划分推迟到解决问题为止。在包括PDAC在内的许多类型的癌症中,辐照后G2检查点被强烈激活,这已显示出增加对治疗的耐药性。
另一方面,自噬是一种自然机制,细胞通过该机制消化了一些自身的细胞器和蛋白质,尤其是受损或不必要的蛋白质,可以收回营养并保持适当的内部条件,以及其他功能。虽然必不可少的健康细胞研究人员发现,放射治疗后,癌细胞的自噬增加,实际上有助于他们忍受和生存治疗。
最有趣的是,由于自噬和G2检查点共享了一些相同的化学信号,因此有人建议这两个过程相互关联。“尽管提出了关系,但辐射后自噬与G2检查点之间相互作用的机械细节尚不清楚。因此,在最近的研究中,我们试图更多地了解这些过程之间的联系,尤其是在PDAC细胞中,尤其是在PDAC细胞之间的联系。”大沼泽博士解释说。
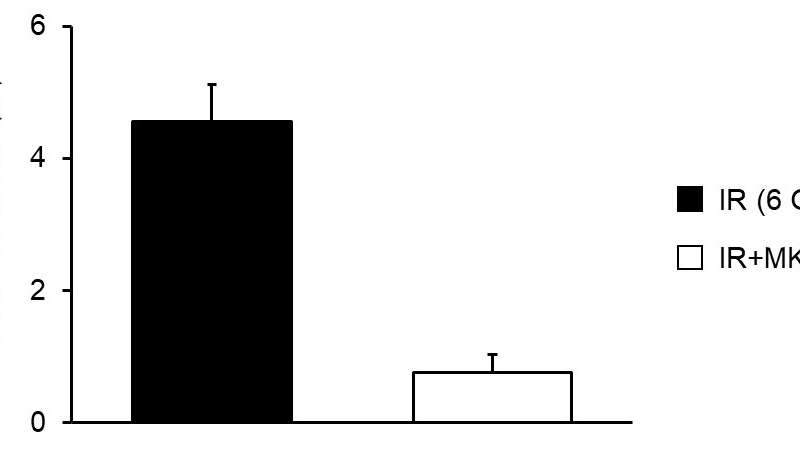
在PDAC细胞培养物中进行了许多实验之后,大谷川博士领导的科学家团队确定辐射诱导的自噬依赖于被激活的G2检查点。此外,他们表明自噬帮助辐照的PDAC细胞产生更多的能量(以称为ATP的分子的形式),这转弯导致了它们的生存。因此,当G2检查点被化学抑制时,团队开始分析辐照PDAC细胞发生的事情。这些无法激活G2检查点的辐照细胞没有进行自噬,因此更可能在放射后死亡。

然后在小鼠中测试了这些有希望的结果,将PDAC细胞移植以产生肿瘤。通过使用辐射和G2检查点抑制剂治疗这些小鼠,与单独施用辐射相比,科学家们大大抑制了肿瘤的生长。从本质上讲,这意味着可以有效地使用减轻自噬的G2检查点的抑制器,以降低PDAC细胞的辐射抗性。哈谷博士总结说:“我们的研究应促进PDAC的放射增感器或新的放射治疗策略的发展。反过来,这可以很大程度上提高这种类型癌症患者的存活率。”
将需要进一步的研究以更好地了解G2之间的联系检查点和自噬以及这些过程如何使癌细胞更具耐药性。让我们希望科学家最终找到有效打击特别困难的方法癌症PDAC等类型,并为受影响的人提供更多的生活。
进一步探索