研究人员从人类诱导的多能干细胞中培养肠细胞
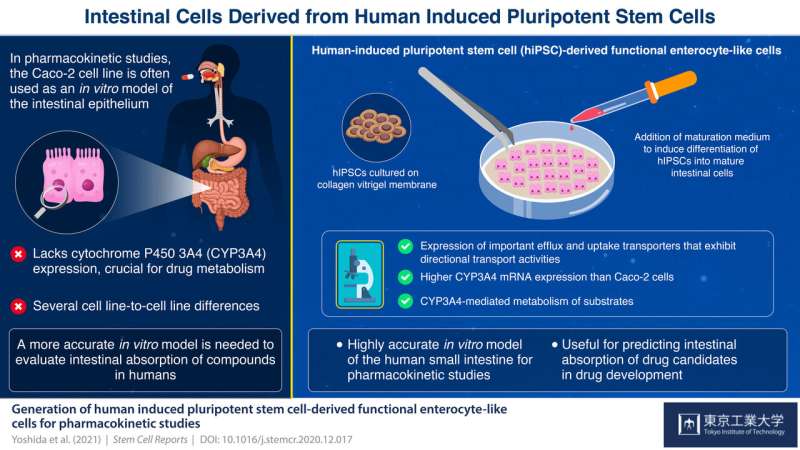
来自日本的科学家团队在生长的小肠细胞中取得了成功,类似于人体中发现的那些来自人类诱导的多能干细胞。科学家使用他们以前在胚胎干细胞上开发的程序进行此发现。他们声称生长的细胞可用于重点是人类小肠药物运输和代谢的实验室研究。
肠上皮细胞位于小肠上皮内,是大多数口服药物的吸收和代谢部位。因此,新型口服药物的吸收研究依赖于体外或动物模型来准确地再现小肠环境。目前,科学家广泛使用人类结肠癌细胞系Caco-2作为肠道上皮的模型。然而,这也有它的缺点:Caco-2细胞来源于结肠;因此,它们更像结肠而不是小肠。例如,这些细胞不表达细胞色素P450 3A4 (CYP3A4),而细胞色素P450 3A4是药物代谢的关键蛋白,在小肠中大量表达。此外,Caco-2细胞倾向于表现出高细胞系到细胞系的变异。
为了解决这些问题,来自东京科技大学东京工业大学,康托化工有限公司,Shionogi&Co.,Ltd,Shionogi Technoadvance Research Co.,Ltd。开发了来自人类的新型肠细胞样细胞- 诱导多能干细胞在适当的生长因子作用下,它可以分化成任何类型的细胞。
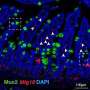
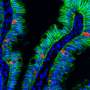
通过修改他们以前用于人类的程序胚胎干细胞,科学家最初延长了称为肠祖细胞的小肠细胞早期阶段的细胞。然后,它们在胶原葡萄酒(CVM)上培养这些祖细胞。此外,它们用含有6-溴吲哚-3'-肟,二甲基亚砜,地塞米松和活化维生素D3的成熟培养基处理了祖细胞。他们的努力导致肠细胞样细胞的发展,其与实际肠细胞紧密相似,表达出现的流出转运蛋白调节药物吸收和CYP3A4,其中Caco-2细胞缺乏。东京工业大学副教授博士博士,以及本研究的相应作者之一增加,“我们通过培养了HIPSC衍生的内胚层或肠祖细胞来从HIPSC产生肠细胞样细胞的有效培养程序CVM上的细胞。“
科学家们声称,这些最早的类似肠细胞的细胞可以用作小细胞的体外模型肠用于评估人类药物的肠道吸收。阐述了使用这些细胞用于未来研究的优势,东京理工学院教授绍恩·凯博士,本研究的联合对应作者,评论,“髋科衍生的肠溶类?细胞本研究所建立的可用于在药物-药物相互作用改变转运体/代谢酶功能等特殊情况下以及在正常情况下的人体肠道药物吸收的定量预测。”
进一步探索












用户评论