诱导的血管祖细胞促进缺血性血管疾病模型的功能恢复
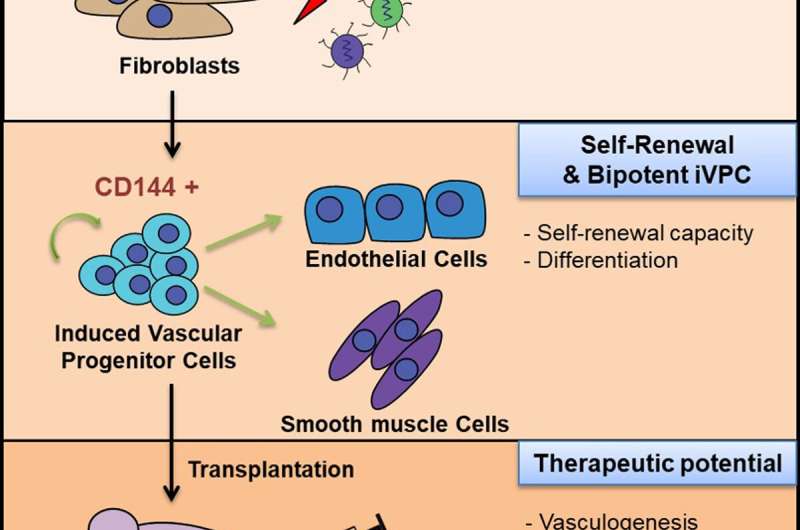
韩国蔚山国家科学技术研究所(UNIST)的一个研究团队通过直接谱系转换成功地生成了双潜能自我更新的ivpc。
革命性的血管先驱细胞(VPCs)用于缺血性血管疾病的治疗已被发现。这是通过直接谱系转换产生的,在大规模细胞培养过程中不太可能导致癌症,因此可以用作3d打印人体组织(如心脏或肝脏)所需血管的主要原料。
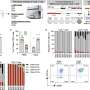
这一突破是由UNIST生命科学学院的Jeong Beom Kim教授和他的研究团队领导的。在这项研究中,研究小组证明了ETS可以从成纤维细胞中产生诱导的VPCs (iVPCs) (e - 26)。转录因子, Etv2和Fli1。此外,该iVPCs移植到缺血后肢模型增强血液流动在体内不形成肿瘤,这为治疗缺血性血管疾病提供了有趣的可能性。
当损坏发生时血管将血细胞,营养物质和氧气运送到身体组织,缺血性血管疾病发生。细胞疗法包括移植细胞以恢复组织或器官功能,作为缺血性疾病的潜在治疗方法受到了广泛关注。血管祖细胞(VPCs),通过多能干细胞(PSCs)的分化产生,包括胚胎干细胞和诱导PSCs (iPSCs),具有自我更新能力,因此非常适合大规模生产。虽然VPCs被认为是治疗缺血性疾病的最强候选者,但移植后残留的未分化细胞可能形成肿瘤,这是psc来源的VPCs应用于缺血性疾病患者的关键障碍。
金教授通过直接谱系转换(直接谱系转换)解决了这一问题。直接谱系转换是指,只使用谱系限制的转录因子,从另一个谱系诱导功能细胞。在这项研究中,研究小组证明了ETS (e - 26)转录因子、Etv2和Fli1可以从成纤维细胞中产生诱导的vpc (iVPCs)。
“Etv2和Fli1的dna主要表达在血管发育的早期阶段,”Soo Yong Park(联合硕士/博士)说。他是该研究的第一作者。“在这项研究中,我们证明了Etv2和Fli1的异位表达足以将成纤维细胞转化为诱导的vpc (ivpc),从而产生ECs和smc。”
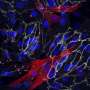
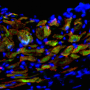
干细胞具有广泛增殖(自我更新)和分化为其他细胞类型(生物潜能)的能力。在这项研究中,研究团队通过直接谱系转换成功地生成了双潜能自我更新的ivpc。他们还证实了iVPCs可以分化为功能性内皮细胞(ivpc来源的内皮细胞)或平滑肌细胞(ivpc来源的平滑肌细胞)在规定的培养条件下。此外,他们还观察到,在缺血性血管疾病模型中,移植的iVPCs可以促进血流而不形成肿瘤。
Kim教授说:“我们证明了缺血性疾病可治愈的ivpc,具有自我更新和双效性,可以通过强制ETS家族转录因子、Etv2和Fli1表达从小鼠成纤维细胞中产生。”“我们的研究可能会促进未来动脉粥样硬化的治疗应用。”
这项研究的结果已发表在该杂志上动脉硬化,血栓形成和血管生物学.
进一步探索