研究人员解开了细胞外囊泡的愈合机制
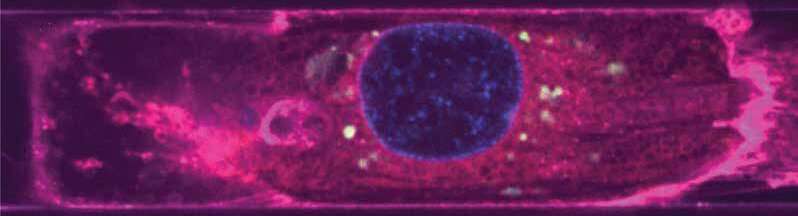
细胞外囊泡(ev)——纳米大小的信使,在细胞之间传递线索和货物——是下一代治疗从自身免疫和神经退行性疾病到癌症和组织损伤的很有前途的工具。来自干细胞的ev已经被证明可以帮助心脏细胞在心脏病发作后恢复,但它们究竟是如何帮助心脏细胞的,以及这种有益的效果是否只针对来自干细胞的ev仍然是一个谜。
现在,来自哈佛大学约翰·a·保尔森工程与应用科学学院(SEAS)的研究人员已经揭示了ev治愈能力背后的潜在机制,并证明了它们不仅能在创伤后使细胞复苏心但在心脏病发作时,在缺氧的情况下保持细胞功能。研究人员在人体组织利用内置传感器的芯片心脏持续追踪组织收缩。
研究小组还证明,这些细胞间旅行者可以从血管表面的内皮细胞中提取,内皮细胞更丰富,更容易维护干细胞.
这项研究发表在科学转化医学。
“我们的器官芯片技术已经发展到可以对抗药物靶点,而不是对抗芯片设计的程度,”该研究的高级作者Kit Parker说,他是SEAS生物工程和应用物理学塔尔家族教授。“通过这项研究,我们用人类细胞在芯片上模拟了一种人类疾病,并开发了一种新的治疗方法来治疗它。”
当流向心脏的血液被阻塞时,就会发生心肌梗塞。当然,最好的治疗方法是心脏病是恢复血液流动但这个过程实际上可能会对心脏细胞造成更多的损伤。所谓的缺血再灌注损伤(IRI)或再氧损伤,发生在组织缺氧一段时间后血液供应恢复。
“细胞对IRI的反应涉及多种机制,比如钙和质子过载,氧化应激海洋工程学院和威斯生物激励工程研究所的博士后莫兰·亚迪德(Moran Yadid)说,他是这篇论文的第一作者。“这一系列复杂的过程对开发有效的疗法提出了挑战,这些疗法可以解决这些问题。”
这就是内皮源性ev (eev)的作用所在。因为这些囊泡来自于血管组织,而血管组织能够独特地感知缺氧压力,研究人员假设它们所携带的物质可以提供直接的保护心肌.
研究人员绘制了由囊泡表达的整套EEV蛋白质。
亚迪德说:“令人惊讶的是,尽管这些囊泡的直径只有150纳米,但它们包含了近2000种不同的蛋白质。”“很多这些蛋白质与代谢过程比如呼吸,线粒体功能,信号传导和体内平衡。换句话说,很多过程都与心脏对压力的反应有关。所以,我们认为外泌体包含的分子和蛋白质的混合物,而不是一个具有治疗作用的分子,它们可以一起帮助细胞维持内稳态,处理压力,修改代谢作用,减少损伤量。”
该团队使用由SEAS的疾病生物物理学小组开发的心脏芯片模型测试了eev对人类心脏组织的影响。芯片上的器官平台模拟了原生组织的结构和功能,并允许研究人员实时观察人体组织中损伤和治疗的影响。在这里,研究人员模拟了植入eev和未植入eev的芯片上的心肌梗死和复氧。
研究人员发现,在eev处理过的组织中,心肌细胞可以更好地适应应激条件,并承受更高的工作量。研究人员通过3小时的限氧和90分钟的复氧诱导损伤,然后测量死亡细胞的比例和组织的收缩力。经过eev处理的心脏组织在受伤后死亡细胞的数量是原来的一半,收缩力是未经处理的组织的四倍。
研究小组还发现,与未处理的细胞相比,使用eev处理的受伤心肌细胞表现出一组与未处理的细胞更相似的蛋白质。令人惊讶的是,研究小组还观察到,即使在没有氧气的情况下,用eev处理的细胞也会继续收缩。
“我们的研究结果表明eev可以保护心脏组织由复氧损伤部分由补充损伤细胞支持不同代谢过程的蛋白质和信号分子,为新的治疗方法铺平了道路,”哈佛医学院病理学客座教授、该研究的合著者André G. Kléber说。
帕克说:“当一个分子、一个靶点的传统模式无法治愈疾病时,外泌体细胞疗法可能是有益的。”“通过我们所使用的囊泡,我们相信我们正在采取猎枪式的方法来打击药物靶点网络。有了我们的器官芯片平台,我们将准备以治疗的方式使用合成外泌体,这可能更有效,更可靠的制造。”