亨廷顿舞蹈症的神经脆弱与线粒体RNA的释放有关
在第一个全面追踪不同类型的脑细胞如何对导致亨廷顿舞蹈症(HD)的突变做出反应的研究中,麻省理工学院的神经科学家发现,一种特别受折磨的神经元的一个重要死亡原因可能是对线粒体(为细胞提供能量的细胞成分)错误释放的遗传物质的免疫反应。
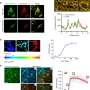
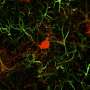
在疾病发展的不同阶段的不同细胞类型中,研究人员测量了死于亨廷顿舞蹈病的人的大脑样本和经过不同程度基因突变改造的小鼠的RNA水平与正常水平的差异。在对这两个物种的几个新观察中,一个特别引人注目的是,来自线粒体的RNA在被称为刺状投射神经元(SPNs)的脑细胞中错位,这些细胞在疾病中受到破坏,导致了致命的神经症状。科学家们观察到这些迷路的rna,它们看起来不同于细胞比RNA的来源细胞核引发了有问题的免疫反应
该研究的资深作者、麻省理工学院大脑与认知科学系副教授、皮考尔学习与记忆研究所副教授、麻省理工学院和哈佛大学布罗德研究所副教授Myriam Heiman说:“当这些rna从线粒体中释放出来时,它们看起来就像病毒rna一样,这会引发先天免疫,并导致细胞死亡。”“我们认为这是引发炎症信号的途径的一部分,这在HD中已经见过了。”
Picower研究员Hyeseung Lee和前访问科学家Robert Fenster是该研究的共同主要作者神经元.
线粒体事故
该团队的两种不同筛选方法,一种是可用于小鼠的“TRAP”,另一种是可用于小鼠和人类的单核RNA测序,不仅在spn中特别发现了线粒体RNA的存在,而且还显示了一种名为氧化磷酸化的过程的基因表达不足,这种过程被称为燃料饥渴的神经元用来制造能量。小鼠实验表明,这种下调氧化磷酸化和线粒体RNA释放的增加都发生在疾病的早期,在大多数其他基因表达差异明显之前。
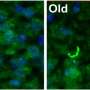
此外,研究人员还发现了一种名为PKR的免疫系统蛋白质的表达增加,PKR已被证明是释放的线粒体RNA的传感器。事实上,研究小组发现PKR不仅在神经元中升高,而且还被激活并与线粒体rna结合。
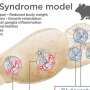
海曼说,新的发现似乎与其他临床疾病相吻合,比如亨廷顿舞蹈症,会导致大脑中被称为纹状体的区域受损。在一种被称为Aicardi-Goutières综合征的情况下,由于先天性免疫反应失调,同样的大脑区域可能会受损。此外,儿童与硫胺素缺乏症患有线粒体功能障碍,之前的研究表明,缺乏硫胺素的小鼠表现出PKR激活,与海曼团队的发现非常相似。
他们在报告中写道:“这些以纹状体细胞死亡为特征的非hd人类疾病,通过将这里描述的氧化代谢缺陷和自身炎症激活现象直接与没有[亨廷顿舞蹈症突变]背景的人类纹状体细胞死亡联系起来,扩大了我们发现的意义。神经元.
其他观察结果
海曼说,尽管线粒体RNA释放的发现是最引人注目的,但这项研究还产生了其他几个潜在有价值的发现。
首先,这项研究产生了基因表达的重大差异的全面目录,包括与重要神经功能相关的差异,如突触电路连接和生物钟功能。另一种基于研究小组对结果的分析,认为神经元中这些基因转录改变的主要调节因子可能是视黄酸受体b(或“Rarb”)转录因子。海曼说,这可能是一个临床有用的发现,因为有药物可以激活Rarb。
海曼推测:“如果我们能抑制转录失调,我们就有可能改变这种疾病的结局。”“这是一个需要验证的重要假设。”
海曼说,这项研究的另一个更基本的发现是,研究人员在人脑样本中的神经元中看到的许多基因表达差异与他们在小鼠神经元中看到的变化非常吻合,这为小鼠模型确实对研究这种疾病有用提供了额外的保证。这个问题在一定程度上困扰着这个领域,因为老鼠通常不像人那样表现出那么多的神经元死亡。
“我们看到的是,实际上小鼠模型概括了这些阶段HD人类发生的基因表达变化神经元很好,”她说。“有趣的是,其他一些非神经元细胞类型在人类疾病和小鼠模型之间并没有表现出那么多的保守性,我们的团队认为这一信息将有助于其他研究人员在未来的研究中。”
单核RNA测序研究是与麻省理工学院计算机科学与人工智能实验室Manolis Kellis团队长期合作的一部分。这两个实验室希望在不久的将来扩大这些研究,以进一步了解亨廷顿舞蹈病的机制。
进一步探索