科学家发现路标在DNA对癌症、疾病风险
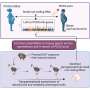
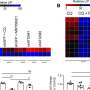
通过测序整个基因组DNA的修改,和分析癌症组织和健康的,哈肯萨克市子午线卫生研究人员和医生发现这可能是癌症和其他疾病的风险的关键:特定位置在这些表达式的DNA改变(甲基化)是不平衡的,根据一项新的出版物。
作者,从发现和创新中心(CDI),哈肯萨克大学医学中心和约翰Theurer癌症中心(JTCC)和美国国家癌症Institute-recognized乔治敦Lombardi综合癌症中心的财团,他们的研究结果发表在主要的杂志基因组生物学6月29日。
最强烈disease-relevant很难定位的遗传变异广泛的基因组图谱,但扫描放大与这些DNA甲基化相关的关键基因的位置在多个正常和失衡癌症组织科学家报告,他们发现了有前途的新线索在更广泛的统计信号。
“我们的密集allele-specific甲基化(即地图。由遗传变异决定),DNA甲基化失衡将帮助其他科学家优先和重点工作最相关的与疾病相关的遗传变异,”凯瑟琳说,医学博士博士,助理CDI的成员,和第一作者。“因为我们还挖了这一现象的机制了解它可以导致疾病的易感性,我们的研究将有助于确定新的有趣的生物通路个性化医学和药物开发”。
“癌细胞是歹徒,但在我们的方法,我们让他们为我们工作在一个有用的方法,”本杰明Tycko说,医学博士博士,CDI实验室主任负责这项研究。“这些“足迹”allele-specific甲基化比正常组织更丰富的癌症,但由于凯瑟琳的研究表明它们是由相同的生物学途径,我们可以使用密集的地图了解癌症的起源和发生自身免疫性疾病,神经,和代谢疾病障碍。”
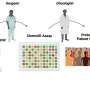
当前的研究产生最大的高质量数据中使用这种方法。DNA样本研究中有各种各样的组织类型从89年健康对照组,加16癌症样本三种类型的肿瘤治疗肿瘤医生和外科医生JTCC: b细胞淋巴瘤,多发性骨髓瘤,多形性成胶质细胞瘤(一种常见的和难治性脑瘤)。
科学家们发现了一个15112 allele-specific甲基化网站包括1838网站统计信号附近疾病易感性的全基因组关联研究(GWAS)。这些数据已经公开,以便其他科学家可以测试“post-GWAS”研究的新假说。
也在其小说研究,本文报告证据表明非编码基因突变(不改变蛋白质序列)“癌症中可能扮演的角色通过远程监管的影响基因表达”。论文中引用一个特定的示例是一个突变,导致TEAD1 allele-specific甲基化基因,这证据表明变得过度积极的和难以形式的多发性骨髓瘤。
另一个发现是,一些disease-relevant基因变异可以驻留在DNA中“染色质沙漠,”地方很少或根本没有特定的生物信号可用组织类型但所透露的足迹allele-specific甲基化在不同的时间和可能是活跃的细胞历史或发展阶段。
“这可能是一个关键的突破在确定癌症开始和给我们一个更好的机会去如何对待它,”大卫·西格尔说,医学博士创始主任多发性骨髓瘤、淋巴瘤CDI研究所和多发性骨髓瘤部门主任约翰•哈肯萨克大学医学中心Theurer癌症中心和报告的作者之一。“寻找非编码基因突变导致表观遗传基因的激活TEAD1等多发性骨髓瘤可能帮助我们缩小的最有前途的发展目标的新疗法。”
“这样的先进的表观遗传研究将推动临床决策在不久的将来,“安德烈异邦人说,医学博士,硕士哈肯萨克子午线,physician-in-chief肿瘤健康和约翰Theurer癌症中心主任,也是该论文的作者之一。”像这样的研究,观察最详细的DNA甲基化和基因表达的变化,可以帮助我们解决这个谜题的癌症开始和也许如何征服它。”
“我赞赏我们理解这一重要贡献癌症和它的潜在生物学可能适用于其他疾病,”路易斯·m·韦纳说,医学博士乔治敦Lombardi综合癌症中心主任和MedStar乔治敦大学癌症研究所。“这项研究发现更多的证据通过结合不同调查人员能够实现机构和专业。”
更多信息:凯瑟琳et al, Allele-specific DNA甲基化密度增加癌症及其映射在正常和肿瘤细胞变异监管snp的产量增加,基因组生物学(2020)。DOI: 10.1186 / s13059 - 020 - 02059 - 3