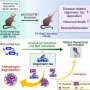
蛋白质的三维结构揭示了阿尔茨海默病毒性的新机制
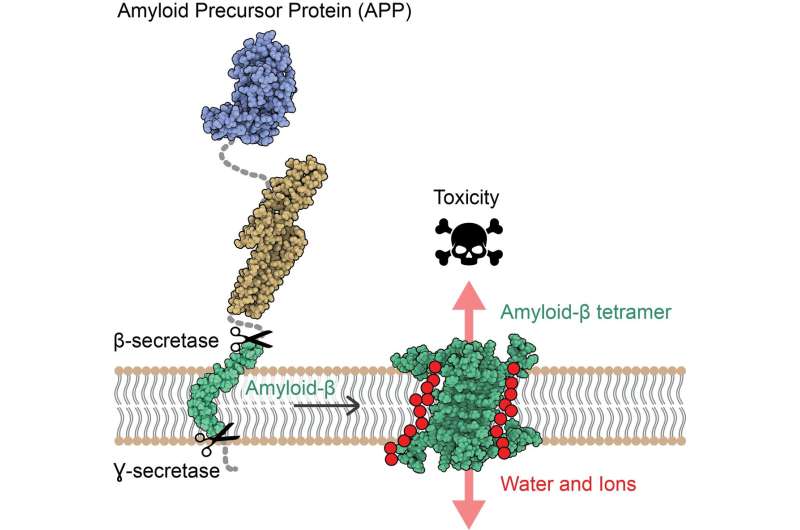
患有阿尔茨海默病(AD)的人的大脑正在缓慢而不可避免地消耗神经元,这导致了与这种疾病相关的记忆和认知功能的特征性丧失。然而,神经元死亡的原因仍然未知。现有的治疗方法旨在减缓痴呆症的发展,只有助于短时间内提高生活质量。因此,治疗阿尔茨海默症是一种未被满足的医疗需求。
由纳塔莉亚·卡鲁拉领导的研究人员,IRB巴塞罗那校友,波尔多Européen de Chimie et Biologie研究所(IECB)的前小组负责人,目前CIEF集团的项目经理首次揭示了β淀粉样蛋白(Aβ)的原子结构。蛋白质组装.对这种结构的了解揭示了这些组合的毒性新机制,具有破坏神经元的能力膜使水和离子通过,导致这些细胞死亡。一些研究已经提出Aβ的相互作用蛋白质导致了AD中观察到的神经元死亡然而,a β蛋白是一个困难的治疗靶点,因为它是“粘性”和自我组装,采用不同的形状和大小。
Carulla解释说:“了解这些蛋白质组合的特征,例如构成它们的分子数量和它们所采用的形状,对于设计有效的治疗策略至关重要,这些治疗策略针对的是导致AD神经毒性的Aβ组合形式。”
确保Aβ稳定形成的体外方法
为了解决构象的不稳定性,研究小组首先在体外研究了Aβ蛋白——在模拟神经元膜的简化模型系统中——以开发条件制备稳定的Aβ形式的均匀组成和形状。一旦确定了这些成分,他们就研究了它们的结构和神经毒性模式,建立了组成a β系综的所有原子的三维排列。
该论文的第一作者Sonia Ciudad和Eduard Puig说:“我们的研究表明,一些Aβ关联可以穿透神经元的膜,改变它们的渗透平衡,从而引发它们的死亡。”Ciudad是IRB巴塞罗那校友,目前是Werfen公司Biokit的研发科学家;Puig现在是巴塞罗那IRB不对称合成研究部门的博士后。
靶向膜孔以避免神经毒性
这项研究强调了两种Aβ蛋白组合,一种由4个Aβ蛋白组成,另一种由8个Aβ蛋白组成,其排列具有破坏细胞膜的能力,提出它们是引起AD神经退行性变的候选者。
进一步的工作应该集中在防止这种集合形成的方法上,从而防止膜破坏。目前,该领域的药物发现管道不包括任何靶向膜相关a β组合的药物,因此这一发现可能是治疗AD的重大突破。