专家对COVID-19患者高凝血率的反应
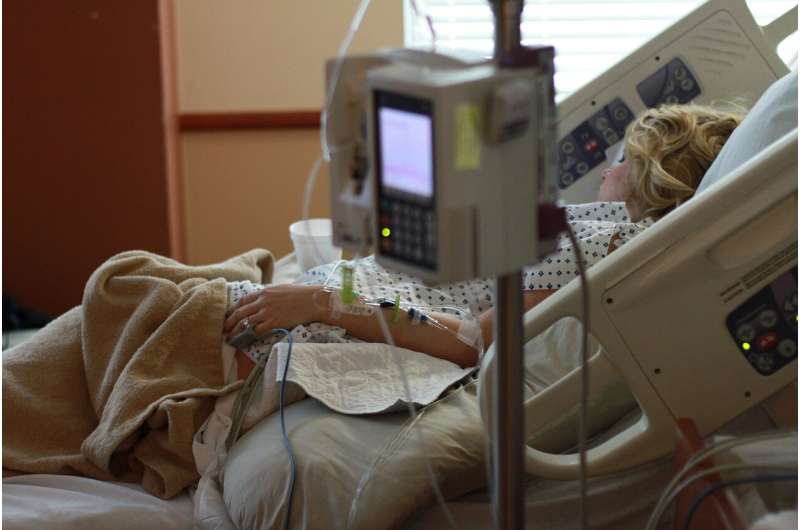
本周早些时候,BBC报道,三分之一的Covid-19患者开发了危险的血栓。虽然目前的治疗主要关注抗病毒和潜在的抗炎治疗,但这些仅解决了病毒的直接影响。如果病毒是洪水,这些治疗方法控制洪水但不考虑造成的损坏。除了治疗免疫系统过度或中和病毒的药物外,迫切需要专注于解决这种凝块形成的药物,包括使用血液稀释剂,以及凝块破坏剂,尤其是正确的剂量和右患者.
是Covid-19患者的“三分之一”的形象是开发血栓的一个现实的一个吗?为什么这很高的比例?
多个国家已经报告了病例系列,在重症监护病人中引用的数字高达40%。在病房的病人也有更高的流行率,即使不是同等规模的重症监护病人。
这多余的血栓形成已在尸检报告中得到证实,在肺部有更广泛的血栓形成,在其他器官的血管中也有血栓形成。
血液凝块与我们在临床实践中经常看到的不同吗?
视图正在开发这些患者中的肺动脉血栓可能代表Novo血栓形成,与代表栓塞现象的典型凝块不同。换句话说,由血管中的新沉积物形成的凝块而不是形成在迁移的身体的其他部分中的块。这可能解释了呼吸困难的缓慢发作。在一些患者中,已经看到了一种更典型的快速发作呼吸呼吸呼吸呼吸呼吸呼吸呼吸呼吸呼吸呼吸困难。
我怀疑两者都是患者组中常见的两种,具有代表De Novo血栓形成的较小的外周血栓。较大动脉中的血栓可能是栓塞的。
血栓形成的治疗策略怎么样?
有一种假设是管理过多的细胞因子和免疫激活可以解决血栓形成。这是一种误解,因为我们对其他血栓形成的情况,包括动脉和静脉血栓形成的经验表明,解决原因并不能清除血栓。凝块通过称为纤溶的周转过程被清除,这是凝血过程固有的。这也可以通过外部药物称为凝块克星(组织纤溶酶原激活剂或链激酶)
在中度炎症继发血栓形成或遗传或获得性继发高凝的背景下,抗凝是主要的治疗方法。首先,它们可以解决凝血系统的后果,即防止血栓的进展和复发。
如果所有患者应接受治疗抗凝剂,也存在相当大的辩论。另一方面,涉及出血的潜在风险。虽然试验不需要筛选,但尽管普遍存在,但仍有一种随机试验正在进行一项随机试验。
非常重视抗病毒和抗炎策略,但是悲伤的研究解决凝血的研究已经努力被糟糕的“重要”。虽然抗病毒和潜在的抗炎策略可以控制“洪水”,即病毒感染和相关细胞因子风暴,“洪水损伤”中,即肺泡和血液中的纤维蛋白需要通过交替机制来解决。
科学家认为什么是导致Covid-19患者血液凝血增加的机制?
一致的发现是升高的D-二聚体,通常可以看到升高4至10倍。此外,在病态患者中,已经看到高达100至150折的增加。升高的D-二聚体与较高的死亡率和发病率有关。与肺病严重程度的关系尚不清楚。
已经提出了几种解释,并且对Covid-19中的过量血栓形成或凝血异常负责的机制并不完全阐明。
可以考虑三种可能的机制。
- 凝血异常可能是细胞因子风暴的次要。这似乎是最普遍的信念,但有趣的是要注意患者在纤维蛋白原或血小板中没有同时降低。通常,细胞因子风暴的凝结病变往往具有低纤维蛋白原,低血小板和升高的D-二聚体的消耗性。
- 第二种可能性是由于肺泡上皮的邻接,内皮受损,并且存在严重炎症,旁观者效果。这种机制可以解释该组患者中可见的过量肺动脉血栓形成。通常在这种情况下,肺泡中的纤维蛋白溶解剂含有溢出血液纤维溶解剂。
- 第三种可能性是内皮细胞的直接感染。有一个案例报告表明这种可能性。.
关于肺动脉血栓形成的研究如何?
CT肺血管造影可以在肺脉管系统中展示血栓,直至亚分段水平。在这些患者中一直挑战,因为它们是呼吸的动作伪成物,并且肺部病理的存在使得较小的血栓更具挑战性,可视化
如果一个人接受肺血栓发展de novo,对于患者不太可能存在更传统的临床症状,它们将变得重要。
在我们的机构,数据审查显示升高的D-二聚体可以预测存在肺动脉血栓形成的存在。
对于最低限度的高d-二聚体患者,大约是正常上限的4 - 6倍,应进行CTPA,抗凝将解决PAT的贡献。
血液凝固可能是什么其他治疗方法?
通常,我们倾向于使用抗凝血剂来管理血栓,但凝块可以用溶血剂裂解。肺栓塞的溶栓可以通过通过外围静脉或导管施用药物作为全身治疗。
有几个静脉注射组织型纤溶酶原激活剂后氧合有短暂改善的病例系列。大多数研究都是在住院接受长期重症监护的患者中进行的,临床结果缺乏效果可能与纤维化有关。也有一项关于雾化组织型纤溶酶原激活剂的研究,看看这是否有助于通过溶出肺泡中的纤维蛋白膜和小血管血栓来改善氧合。











用户评论