霉菌会破坏肺部的保护屏障,从而诱发哮喘
美国威斯康星大学麦迪逊分校的研究人员发现了一种普通曲霉菌诱发哮喘的新方法,即首先攻击肺部深处的保护组织屏障。
在小鼠和人类中,对这种初始损伤的特别强烈的反应与对未来暴露于霉菌的过度反应和呼吸道收缩的特征有关哮喘.
该工作为理解和潜在地阻止哮喘发展提供了新的研究途径,这影响了2500万美国人。模具敏感性占哮喘反应的一定区,因此防止身体建立过敏反应发霉可显著减轻疾病负担。
威斯康辛大学麦迪逊分校儿科、医学、医学微生物学和bob电竞免疫学教授布鲁斯·克莱因和博士后研究员达林·威斯纳3月3日在该杂志上发表了他们的研究结果细胞宿主和微生物.他们与芝加哥大学、明尼苏达大学和哈佛医学院的研究人员合作完成了这项工作。
“曲霉无处不在,它无处不在,我们每一次呼吸都会吸入孢子,”克莱因说。研究小组开始研究这些原本无害的霉菌是如何使某些个体对它们的孢子产生强烈的哮喘反应的。
模具的消化酶是一个自然的目标。霉菌在腐朽物质上饲喂它们的环境中,将这些酶分泌到其环境中的蛋白质。一种这样的酶,一种称为ALP1的蛋白酶是已知的肺过敏原并用曲霉菌模具大量分泌。但ALP1如何诱导哮喘一直是一个谜。
威斯纳研究了Alp1是否能在体内触发一系列已知的过敏反应途径。但他没有找到任何证据表明Alp1曲霉激活了这些过敏反应,这些过敏反应通常会对有害微生物的独特特征做出反应,比如病原体。
威斯纳说:“认为这些非主要病原体的无处不在的真菌可能进化出高度特定的成分的想法似乎没有道理。”“因此,人们吸入肺部的这些蛋白酶只会造成损害,这似乎更合理。当它们进入人类和老鼠的肺时它们首先与之互动的是上皮细胞."
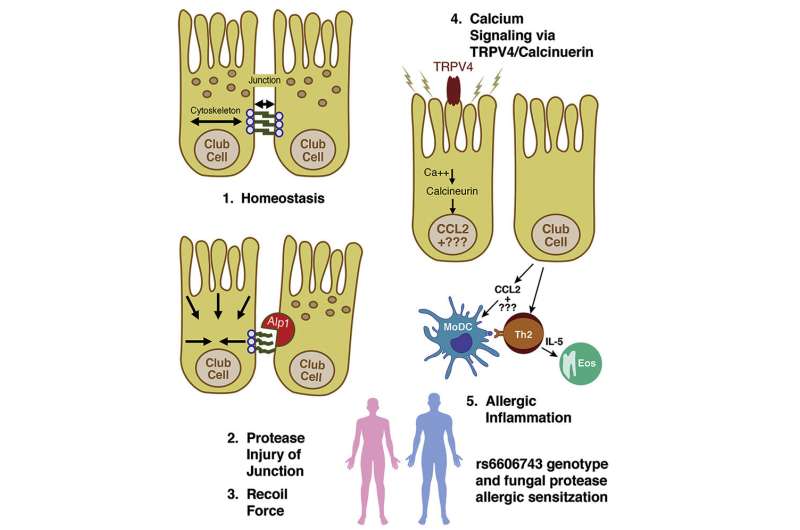
因此,Wiesner寻找10种肺上皮中的哪一个细胞组成肺部表面,对ALP1损坏最强烈的反应。他在被称为俱乐部细胞的人中归零。俱乐部细胞主要位于支气管中,最小的气道通道,气体与血液交换。众所周知,俱乐部细胞试图从肺部擦洗污染物,因此在响应模具等环境攻击时的作用是有道理的。
像所有的肺细胞一样,俱乐部细胞紧紧地与周围的细胞结合在一起,在肺和身体的其他部分之间形成一道屏障。这些连接是由蛋白质构成的,而Alp1是用来攻击和消化蛋白质的。威斯纳发现,将小鼠暴露在Alp1环境下会导致肺屏障渗漏,这是Alp1破坏这些细胞连接的证据。
在寻找身体如何感受到这种受损的障碍时,Klein的团队转向哮喘学习的童年起源,由UW-Madison科学家领导,这些科学家们遵循数百名儿童,以确定哮喘的遗传和环境原因。他们发现,称为TRPV4的基因附近的突变,其增加了由身体产生的TRPV4蛋白的量,与儿童的霉菌哮喘相关。
老鼠也产生TRPV4。当威斯纳在小鼠俱乐部细胞中删除该基因时,它们对Alp1的敏感性大大降低。当他诱导俱乐部细胞产生更多TRPV4时,小鼠对霉菌酶过敏。
TRPV4感测细胞的物理变化,并释放出一波钙,然后由其他细胞组分感测。钙是一种常见的细胞信号,但是在过去产生了在生产哮喘中发挥作用的钙的少数证据。
Klein的团队现在认为Alp1攻击肺细胞之间的关节,使细胞挤压。TRPV4感知运动和信号,帮助修复肺部重要屏障的损伤。在有额外TRPV4的小鼠或人类体内,这种反应强烈到足以引起身体的过度反应。这种过度的反应使得肺部在下次遇到Alp1时的反应过于强烈。由此产生的炎症就像哮喘一样。
本研究首次揭示了trpv4 -钙通路在哮喘发病过程中的作用,为抑制和预防哮喘对霉菌的反应提供了新的研究思路。现有药物可以阻断这种钙通道,但要在正确的时间将它们定位到正确的细胞,以防止肺部对无害的霉菌反应过度,则需要更多的工作。
威斯纳说:“以前的药物试验结果令人失望,但这些都是大锤式的方法,他们只是给药钙通道阻滞剂,会阻塞气道中的每个钙通道。”“在这里,我们认为,针对特定细胞的这些药物可以提供针对导致哮喘的有害过度反应所需的特异性。”
进一步探索












用户评论