发现可能会阐明动脉粥样硬化与衰老之间的缺失联系

来自杨百翰和妇女医院的调查人员通过跳入基因组黑暗面的深渊,做出了令人兴奋的发现。曾经被视为“垃圾DNA”,大约75%的人类基因组不会为蛋白质编码。但是,基因组的这些黑暗区域远非垃圾 - 目的是对疾病状态有诱人的线索。由医学博士分庭马克·费恩伯格(Mark Feinberg)领导的一支杨百翰调查员,哈佛医学院的医学副教授,最近陷入了这些地区,以寻找有关动脉粥样硬化的线索 - 这种疾病越来越多地疾病,其中这种疾病变得越来越多硬化和狭窄,阻碍血液流动并导致心脏病。Feinberg及其同事使用了动脉粥样硬化的临床前模型,发现了一个长而非编码的RNA(LNCRNA),该模型可能指向了针对动脉粥样硬化的新疗法的道路,并阐明了为什么疾病的可能性随着年龄的增长而增加。结果发表在科学翻译医学。
Feinberg说:“我们已经确定了一个新的演员控制血管壁上的衰老,令人惊讶的是,它不是传统的基因或蛋白质。它是非编码基因组的一部分。这是出乎意料的。”“我们对胆固醇和炎症在心脏病中的重要性有很多了解,但这是一种新的,额外的途径。我们需要仔细考虑它可能如何影响心血管疾病治疗疗法的发展。”
Feinberg及其同事使用了动脉粥样硬化的小鼠模型,其中小鼠在12周时开始发展动脉粥样硬化病变。研究人员将RNA从血液的内部衬里分离出来船墙并看着整个基因组在所有RNA中,搜索哪些人在疾病进展或回归期间的活动发生变化。最动态的之一是SNHG12,这是一条长长的RNA,不为蛋白质编码,而是在包括人类,猪和小鼠在内的多种物种中发现的。
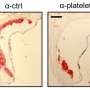
为了更好地了解SNHG12的角色,研究人员进行了实验,他们要么击倒了其活性,要么将其加剧。他们发现,较少的SNHG12导致动脉粥样硬化的大幅增加,但SNHG12大幅度降低了疾病的进展。为了了解SNHG12在做什么,团队正在寻找合作伙伴是谁。事实证明,其中一个是与DNA损伤修复和衰老有关的分子。如果没有这些伴侣一起工作,船只墙就会变得漏水并渗透到坏胆固醇中。该团队可以通过添加一个促进DNA损伤修复的小分子来扭转这一现象,这表明潜在的治疗途径可以追求。
Feinberg说:“真正令人兴奋的是RNA疗法(在我们提供的RNA分子或可以帮助调节RNA的小分子)中是一个增长的区域。”“我们的工作有助于为动脉粥样硬化寻求这种疗法奠定基础。”
进一步探索