靶向药物输送到肿瘤细胞微胶囊

一组科学家从彼得大帝圣彼得堡理工大学(SPbPU)和他们的同事们一起开发了一种靶向药物输送到肿瘤细胞的方法。这一发现是基于对间充质干细胞的使用和微胶囊的高分子化合物。结果发表在生物材料科学日报》。在未来的发现可能允许更精确的治疗肿瘤在不损坏健康的组织。
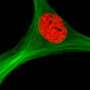
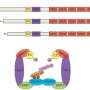
不同类型的组织,包括脂肪、肌肉、软骨和骨,源自间充质干细胞(MSC)。此外,这些细胞可以迁移到肿瘤和反应。这样做的原因是chemokines-protein-like物质正在积极发布的肿瘤。趋化因子吸引特定的细胞表面受体,和这些细胞的迁移与趋化因子浓度的增长。趋化因子受体CXCR4受体表面的MSC与SDF-1趋化因子,使细胞反应接近肿瘤。
“药物输送系统的开发基于活细胞在生物医学是一个燃烧问题。这个策略提供了细胞培养的使用能够与肿瘤反应。msc被认为是最有前途的一个潜在的药物中交付平台,因为他们是相对容易获得和成长在一个实验室,”解释Timofey卡尔波夫,协作开发的方法,在实验室助理微型胶囊和控制交付生物活性化合物,RASA-SPbPU中心。
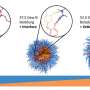
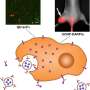
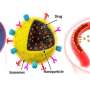
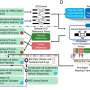
新技术允许一个包在一起不同的生物活性物质,包括抗癌药物。团队选择长春新碱作为样本药物,因为它影响不同类型的生长,并积极使用化疗。长春新碱是放在特殊的高分子化合物制成的微胶囊和金纳米棒。通过吞噬作用胶囊进入了msc,在那之后的细胞治疗红外线深深穿透组织没有损坏它们。因此,黄金微粒胶囊吸收大量的能量和加热。热破坏了聚合物结构,药物被释放到msc。一些长春新碱仍在,但有些也进入细胞间隙,影响了肿瘤。
“新技术的合成子任务和微米大小的聚合物胶囊的包装提供了不同的生物活性物质。在此基础上,平台的广泛的抗肿瘤物质可以开发,和药物可以创建不同地区的现代医学。红外线很长一段时间得到了广泛的应用,几乎是无害的,当辐照参数设置正确,“Timofey卡尔波夫说。
有针对性的药物输送可以帮助减少化疗的毒性作用通过最小化的负面影响健康吗细胞。
更多信息:阿尔伯特·r·Muslimov et al,仿生药物输送平台基于间充质干细胞浸满light-responsive亚微米大小的运营商,生物材料科学(2019)。DOI: 10.1039 / C9BM00926D