研究破译预防2型糖尿病的基因功能

由赫尔辛基大学和牛津大学的研究人员领导的一项国际研究合作已经确定了遗传变异预防2型糖尿病的生物机制。
这项研究发表在该杂志上自然遗传学一项研究发现,锌转运蛋白基因的改变可以降低患2型糖尿病的风险糖尿病通过增强胰腺的胰岛素分泌。
2型糖尿病影响着全球近4亿人。它是由生活方式的结合以及遗传因素两者共同导致高血糖。
其中一个遗传因素是一种名为SLC30A8的基因变异,这种基因编码一种携带锌的蛋白质。这种蛋白质很重要,因为锌对于确保胰岛素(唯一可以降低血糖水平的激素)在胰腺的β细胞中具有正确的形状是必不可少的。
近十年来,研究人员已经知道这种基因的改变可以降低患2型糖尿病的风险,但不知道这是如何发生的。他们现在从患有艾滋病的家庭中招募新成员罕见的基因突变SLC30A8基因,以研究它们对食物中的糖的反应。
“我们研究的一个明确优势是我们可以研究家庭。我们可以将有突变的人与他们没有突变,但遗传背景和生活方式相似的亲属进行比较,”赫尔辛基大学医院的主任医生Tiinamaija Tuomi说,他是这项研究的联合负责人。
“通过这种方式,我们可以确保我们所看到的影响肯定是由于这种基因,而不是由于另一种基因或生活方式因素。”
结果显示,携带这种基因突变的人胰岛素水平更高,血糖水平更低,从而降低了患糖尿病的风险。
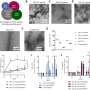
一个国际合作50名研究人员还在实验室中研究了有突变和没有突变的胰腺细胞,并在小鼠和人类细胞材料中进行了实验,以了解当SLC30A8基因功能改变时究竟发生了什么。
“这项工作是一项共同努力将制药和学术界以及来自多个欧洲国家的研究人员聚集在一起。这是一项杰作,因为我们能够测量突变对许多不同系统的影响,包括人类β细胞,”牛津大学惠康人类遗传学中心的安娜·格洛因教授说,她是这项研究的联合负责人。
“我们发现,这种突变对胰腺β细胞的关键功能及其发育过程产生了附带后果。重要的是,这项研究揭示了特定基因变异背后的非凡分子复杂性,赋予了患2型糖尿病的风险或保护,”牛津大学牛津糖尿病、内分泌学和代谢中心的共同第一作者Benoit Hastoy博士说。
赫尔辛基大学芬兰分子医学研究所(FIMM)的共同第一作者Om Prakash Dwidedi说:“总的来说,人体和模型系统的数据表明,葡萄糖刺激的胰岛素分泌增强,同时前激素胰岛素原转化为胰岛素的增强,是预防2型糖尿病的最有可能的解释。”
更好地了解糖尿病背后的遗传和病理机制可以为预防或治疗2型糖尿病开辟新的途径。
“我们的研究结果将这种锌转运蛋白定位为抗糖尿病治疗的一个有吸引力和安全的靶点。如果能开发出一种药物来模仿这种突变的保护作用,那么β细胞的功能就能被保留下来胰岛素分泌指导这项研究的赫尔辛基大学和隆德大学的莱夫·格鲁普教授说。