研究指出了对抗癌症的新靶点
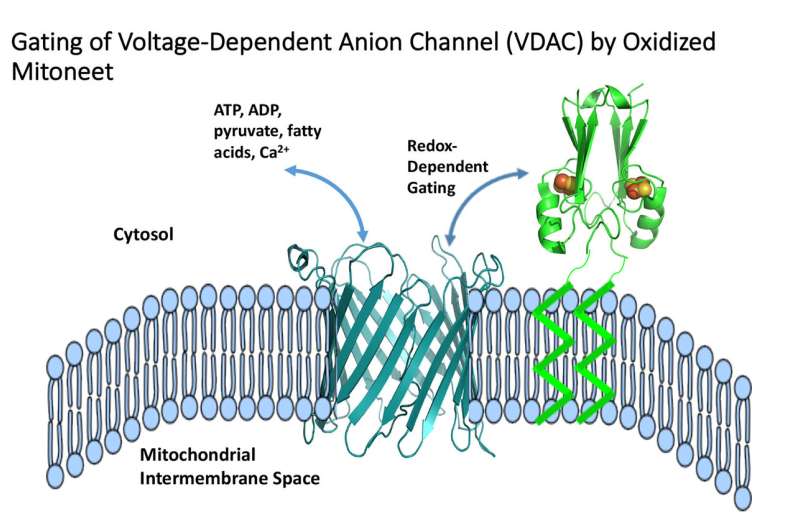
研究人员发现了一种潜在的抗癌新药靶点。
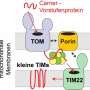
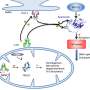
在本周的一项研究中美国国家科学院院刊在美国,一个国际研究团队描述了一种与癌症相关的蛋白质mitoNEET如何关闭线粒体外表面的主要通道,线粒体是供应蛋白质的“发电厂”细胞用化学能。这些通道,或“电压依赖性阴离子通道”(vdac),通常打开和关闭,允许代谢物和其他小分子在线粒体和细胞的其他部分之间通过。
“VDAC通道在细胞质和线粒体之间运输所有类型的代谢物,”该研究的合著者José Onuchic说,他是莱斯大学理论生物物理中心(CTBP)的物理学家和联合主任。“这个通道的功能障碍涉及许多疾病,包括癌症和脂肪肝."
这项研究是由来自CTBP、加州大学圣地亚哥分校(UCSD)、耶路撒冷希伯来大学和密苏里哥伦比亚大学的计算和结构生物学家组成的国际团队进行的。
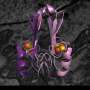
在这项研究中,他们详细介绍了mitoNEET如何调节VDAC,并表明两种蛋白质之间的高亲和力相互作用可以被一种靶向VDAC的药物破坏。
“在健康细胞中自然发生的还原状态下,mitoNEET对VDAC没有可测量的亲和力,”德克萨斯州癌症预防与研究所(CPRIT)癌症研究学者Onuchic说,他领导了Rice在该项目上的努力。“这表明相互作用的机制是氧化还原依赖的,并且在疾病状态下,高度重要的VDAC复合物的靶向可以微调。”
MitoNEET在癌症、糖尿病、衰老和帕金森病中扮演着重要角色,是NEET家族蛋白质的一员,它在细胞内运输铁和硫分子簇。这些簇通过控制还原-氧化或氧化还原过程和代谢来帮助调节细胞。
MitoNEET自然地附着在线粒体的外表面,研究人员表示,MitoNEET与线粒体外膜中最丰富的蛋白质之一VDAC的直接连接具有重要意义。
合著者、加州大学圣地亚哥分校的结构生物学家Patricia Jennings说:“mitoNEET直接打开线粒体的主要孔蛋白VDAC的发现,以及伴随的结构分析和对这种相互作用的预测,为研究在癌症特异性的、受调控的过程中诱导癌细胞发生细胞自杀或凋亡/铁ptosis的方法提供了一个新的平台。”
癌症进展的一个决定性特征是细胞代谢的改变。该研究的合著者、希伯来大学的Rachel Nechushtai说,这项工作表明,有可能通过一种或多种药物来调节VDAC的代谢和功能相互作用,这些药物可能有助于治疗多种疾病癌症.
Onuchic说:“微调一种药物,专门改变VDAC和mitoNEET之间的氧化还原状态,将允许开发对抗多种癌症的新武器。”
Nechushtai和Jennings在2007年首次详细描述了mitoNEET的分子结构,该项目的许多合作者已经在一起工作了十多年,以破译mitoNEET和相关蛋白质(如naf1和MiNT)的工作原理。
密苏里大学的合著者罗恩·米特勒说:“铁和氧化还原的结合是控制许多不同细胞过程的关键,这些细胞过程涉及许多人类病理。”“确定由mitoNEET-VDAC相互作用介导的这些过程的调控主控点是我们对这些过程理解的重要一步。”
研究人员表示,合作者之间的长期联系以及来自美国和以色列的联合资助对该项目的成功发挥了关键作用。
进一步探索