组合疗法显示出复发小细胞肺癌患者的早期希望

PARP抑制剂Olaparib(lynparza)与化学治疗剂Temozolomide(Temodar)结合使用,根据IN阶段I/II期临床试验的结果,在复发小细胞肺癌(SCLC)患者中显示出临床疗效。癌症发现,美国癌症研究协会杂志。
“小细胞肺癌症,占所有肺癌的约15%,历史上的结果很差,这种侵略性癌症类型需要新颖的治疗策略。马萨诸塞州的马萨诸塞州综合医院癌症中心。“这种组合疗法表现出令人鼓舞的SCLC患者的令人鼓舞的结果,这代表了这些通常几乎没有有效治疗方案的患者的新潜在治疗策略。”
Farago指出,在临床前SCLC模型和早期试验中,使用PARP抑制剂在临床前SCLC模型和早期试验中的临床功效有限。她说,但是,添加诸如替莫唑胺等烷基化剂之类的DNA伤害剂可能会增强PARP抑制剂的活性。
这项单臂试验在2015年10月至2018年4月之间招募了50名先前治疗过SCLC的患者;先前治疗线的数量范围从一到七个,有两个先前治疗的中位数。13例患者参加了I期剂量降低研究,其主要目的是确定建议的II期剂量(RP2D)。在RP2D处,将37例患者纳入II期剂量膨胀部分,其主要目的是评估疗效。
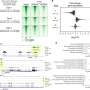
患者在21天周期中的第一至第七天服用了口服Olaparib和Temozolomide;重复该周期,直到疾病进展或不可接受的毒性。在I期部分评估了四个剂量水平,RP2D每天两次确定RP2D为200mg Olaparib,使用75mg/m2每天一次替莫唑胺。
在研究的两部分中,在48名可评估患者中的总体反应率(ORR)为41.7%(20个部分反应,没有完整的反应)。在参与研究的所有50名患者中,无进展的中位生存期和总生存期中位数分别为4.2个月和8.5个月。在RP2D治疗的可评估患者中,ORR为41.0%。
在研究的两个臂中,最常见的治疗相关不良事件(AES)是血小板减少症(患者68%),贫血(占患者的68%)和中性粒细胞减少症(占患者的54%)。在研究的第二阶段部分发生了两级AE,可能归因于研究药物(一种是由于肺炎引起的,另一个是由于中性粒细胞减少症引起的)。
法拉戈指出:“这两个不良事件表明,我们必须告知患者可能的毒性,并在整个治疗过程中努力监测血液计数。”“尽管我们的协议最初没有提供增长因素支持,但通常用于化学疗法方案为了支持中性粒细胞计数,随后对该方案进行了修订,以允许在治疗周期中的第七天使用生长因子支持。”
为了鉴定可能预测对Olaparib-Temozolomide组合反应的分子特征,研究人员在32例患者衍生的异种移植物(PDX)模型中进行了共同临床试验。研究人员确定,四个炎症反应基因(CEACAM1,TNFSF10,TGIF1和OAS1)的特定分子特征可以在发现和验证同类中将敏感模型与抗性模型区分开。此外,这些基因的基础表达低与对研究组合和铂依托泊苷的抗性有关,铂依托泊苷是SCLC患者的标准一线化学疗法。
“尽管已经确定了几种癌症的药物反应生物标志物,但我们没有任何良好的生物标志物的反应小细胞肺癌马萨诸塞州综合医院癌症中心的肿瘤学家本杰明·德拉普金(Benjamin Drapkin)说,“我们在动物模型中的共同临床试验是确定对这两种标准的潜在预后签名的重要第一步。一线化疗和我们的研究组合。”
Farago指出:“这种组合显示了复发性小细胞肺癌患者的显着临床活性,并在一项随机研究中进行了对Olaparib加上替莫唑胺与标准护理选项进行比较的随机研究。”
Farago解释说,由于试验的单臂性质,这些结果无法直接与此环境中的其他治疗选择进行比较。
进一步探索