学分:CC0公共领域
2006年,科学家们发现了一种“重编程”成熟细胞的方法 - 例如,皮肤细胞会产生原则上会产生体内任何组织或器官的干细胞。许多人认为这只是时间问题,直到这种开创性的技术进入诊所并引入了再生医学革命。
因为同一病人既是捐助者,又是细胞来自这些所谓的诱导多能干细胞(IPSC),这些单元将被视为“自我”免疫系统,思想发生了,不遵守困扰常规移植的拒绝问题。
但是,由于无法预料的挫折,IPSC并未成为最初设想的所有治疗方法,其中包括令人惊讶的临床前发现,即IPSC衍生细胞移植通常被拒绝,即使被重新引入了生物体后,细胞是从产生的。
科学家一直在努力理解为什么会发生这种拒绝。但是,加州大学旧金山分校移植和干细胞免疫生物学(TSI)实验室的一项新研究与国家心脏,肺和血液研究所(NHLBI)和斯坦福大学的移植基因组学实验室合作,表明成人对成人的表明-IPSC转化过程可以突变在称为线粒体的微小细胞结构中发现的DNA。这些突变然后可以触发一种免疫反应,从而导致小鼠和人类拒绝IPSC,并更普遍地干细胞移植。
“在再生医学领域,线粒体的作用在很大程度上被忽略了,但是我们实验室的较早努力表明,它们可能会影响干细胞移植的结果。并于8月19日出版了这项新研究的首席作者自然生物技术。“重要的是要了解它们的作用,以便我们能够可靠地控制我们的工程细胞,并确保可以将干细胞产品移植到患者中而不会被排斥。”
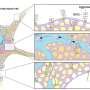
线粒体通常被称为电池的动力室,产生几乎每个生物过程的能量(细菌,没有线粒体,是例外)。但是线粒体是特殊的,原因是另一个原因:它们包含自己的基因组。
之所以称之为“核”人类基因组,是因为它驻留在细胞核中,其中包含超过20,000个蛋白质编码基因和30亿个DNA碱基,这是构成遗传密码的四个字母的化学字母。相比之下,人线粒体基因组仅包含13个蛋白质编码基因,较少含有17,000个碱基。但是,在能量高需求的组织中,小细胞体基因组可能对细胞的总蛋白质含量不成比例。
“在从事大量工作的细胞中,像心肌细胞一样,该细胞产生蛋白质的mRNA分子的三分之一是线粒体的。这意味着单个线粒体突变的负担可能很大。最终只有几种蛋白质可能会引起免疫反应 - 您最终会得到数千个蛋白质。
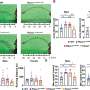
为了表明这种线粒体突变可以触发免疫反应,科学家从一种小鼠菌株和线粒体DNA从另一个小鼠菌株和线粒体DNA产生了杂化干细胞。他们用相同的核DNA将这些细胞移植到小鼠中,但线粒体DNA在两个蛋白质编码基因中的单个碱基不同。移植后几天,他们从小鼠那里收集了免疫细胞,并将细胞暴露于各种线粒体蛋白片段中。引发反应的唯一蛋白是由两个“外源”线粒体基因产生的蛋白质。
尽管不能在人类中进行类似的实验,但科学家还是能够设计出聪明的解决方法。Deuse说:“我们招募了肝脏和肾脏移植患者,并设计了实验,这些实验利用了供体和受体的线粒体DNA自然存在的序列差异。”
与小鼠实验一样,研究人员将免疫细胞与每个移植受者(在这种情况下六个月后)分离,并将细胞暴露于线粒体蛋白片段。结果是相同的:受体的免疫细胞仅是由起源于器官供体的“外来”线粒体蛋白触发的。
Schrepfer说:“在小鼠和人类中,即使是一个线粒体突变也足以具有可识别的免疫反应。”
但是仍然存在一个重要的问题:IPSC衍生的细胞的表现与肝脏和肾细胞相同吗?
事实证明,IPSC转化过程是高度诱变的,并引起了许多新的免疫激活线粒体突变。“在正常的生理条件下,线粒体DNA比核DNA易受突变的10至20倍。将成年细胞转化为干细胞是一个严峻的过程,因此我们预计突变速率同样高或更高。”
此外,与核不同,线粒体缺乏修复DNA的分子机制。取而代之的是,身体依靠免疫系统来发现和破坏产生不熟悉的线粒体蛋白的细胞,这是线粒体DNA已突变的明显迹象。
Shrepfer说,但是变成IPSC的细胞是在体外重新编程和生长的,并且不会通过免疫系统进行除草过程。“我们不会在有机体中制作IPSC,而是在没有免疫监视的情况下将它们制成培养皿。我们培养这些细胞的时间越长,引入新突变的机会就越大,或者是非常罕见的突变的机会已经在场的人将被放大。这使得IPSC在移植时更有可能被拒绝。”
研究的合着者汉娜·瓦兰丁(Hannah Valantine),医学博士,其实验室进行了遗传测序以鉴定这些线粒体DNA突变,他说这些发现可能会对移植领域产生重大影响。
“这项研究揭示了一种可能被拒绝移植的新机制,并可能在将来杠杆化,以发展更好的诊断和免疫抑制剂,”在NHLBI的内血管移植基因组学实验室的首席研究员瓦兰特(Valantine)说,”美国国立卫生研究院的一部分。
Deuse和Schrepfer说,但是IPSC移植并没有注定以前发现一种制作方式IPSCS“无形”到免疫系统 - 一种可以确保IPSC和其他的技术干细胞线粒体突变没有拒绝。但是,如果没有这种隐形斗篷,这项新研究表明,临床医生可能需要对线粒体突变进行仔细的筛查,然后再进行干细胞疗法。
“最重要的是,我们想让人们意识到这种现象。仅仅因为IPSC是从您自己的单元中得出的,并不一定意味着他们不会诱导免疫反应,” Schrepfer说。“在IPSC生产过程中引入突变非常容易,因此在移植之前对IPSC和干细胞产物进行治疗的筛查至关重要。”
CRISPR基因编辑使干细胞“不可见”免疫系统
更多信息:IPSC的线粒体DNA中的从头突变在小鼠和人类中产生免疫原性的新外皮,自然生物技术(2019)。doi:10.1038/s41587-019-0227-7,,,,nature.com/articles/S41587-019-0227-7
期刊信息:自然生物技术
由...提供加利福尼亚大学旧金山