多能-分化转变的机制
诱导多能干细胞可以变成体内任何类型的细胞,也可以保持其原始形态。在当前的版本分子细胞,来自亥姆霍兹中心München的科学家描述了细胞如何决定这两个方向中的哪一个。在他们的研究中,他们发现了一种蛋白质和一种核糖核酸(RNA)在这一过程中起着非常重要的作用。他们的发现也使人们更好地了解肌萎缩性侧索硬化症(ALS),这是一种影响运动神经元的进行性神经系统疾病。
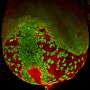
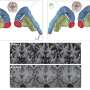
由于它们有能力转化为体内任何类型的细胞,诱导多能干细胞(iPS细胞)可以为再生医学做出关键贡献。例如,为了产生用于治疗1型糖尿病的人工β细胞,必须了解其背后的机制细胞分化.来自亥姆霍兹中心(München)干细胞研究所(ISF)的Micha Drukker博士和他的团队现在已经展示了这些过程是如何在分子水平上控制的。这一切都始于细胞核中的一种结构,这种结构在荧光显微镜的帮助下可见。
细胞核中的两个关键因素
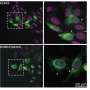
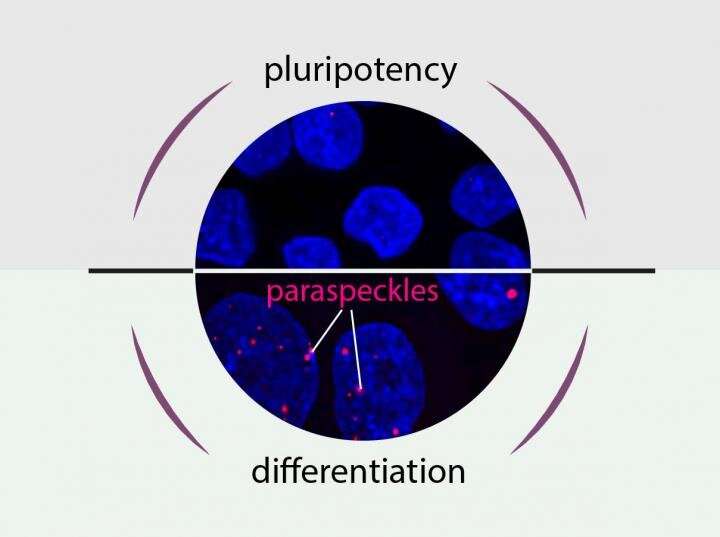
“我们注意到,名为paraspeckles的核结构域不会出现在iPS细胞中,而是在分化过程中迅速形成,与我们创建的细胞类型无关,”德鲁克博士工作组成员Miha Modic博士说。德鲁克和莫迪克假设,这种现象与干细胞分化成体细胞的能力有关。与伦敦大学学院(University College London)的Ule Jernej教授和德鲁克博士团队的博士生马库斯·格罗施(Markus Grosch)一起,研究人员在细胞核中发现了协调副斑的出现以及它们如何调节分化的关键分子。
“在决定细胞是否分化或保持多能性时,有两个因素起着关键作用,”德鲁克说。“我们确定了NEAT1, a核糖核酸(RNA)和TDP-43,一种与RNA结合的蛋白质。”NEAT1有两种形式。短的形式是稳定的TDP-43,在这种情况下,没有旁斑的发展。细胞保持多能性,没有改变。相反,TDP-43的减少会产生长形式的NEAT1。旁斑形成,iPS细胞开始分化。Modic补充说:“这种控制系统可能是干细胞选择何时分化的通用系统。”
Modic说:“糖尿病与再生研究所(IDR)的Silvia Schirge博士和Heiko licert教授帮助我们证明了旁斑对小鼠胚胎发育期间的有效分化也至关重要。总之,他们的研究为理解分化和发展过程提供了一个突破。
与疾病的联系
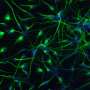
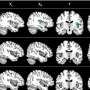
在德鲁克看来,这些发现不仅仅是对基础研究的贡献。他解释说:“旁斑与许多疾病有关,但到目前为止,它们很少在发育和干细胞生物学的背景下被检查。”在这种情况下肌萎缩性侧索硬化症(ALS), tdp -43的作用——以及副斑的出现——尤其明显。在运动神经元中细胞TDP-43受到奇怪的调节,形成有毒的聚集物;长型NEAT1的发生率增加,可检测到更多的旁斑。这些机制被认为是als的早期迹象——甚至在患者出现临床相关症状之前。在下一阶段,Drukker和他的科学家团队希望检查其他类型的细胞,寻找旁斑,rna及其相互作用。到那时,新发现的分子是否能为药物治疗提供合适的靶点也将显而易见。
进一步探索