工程化的“自杀基因”可以提前为1型糖尿病进行细胞替代疗法
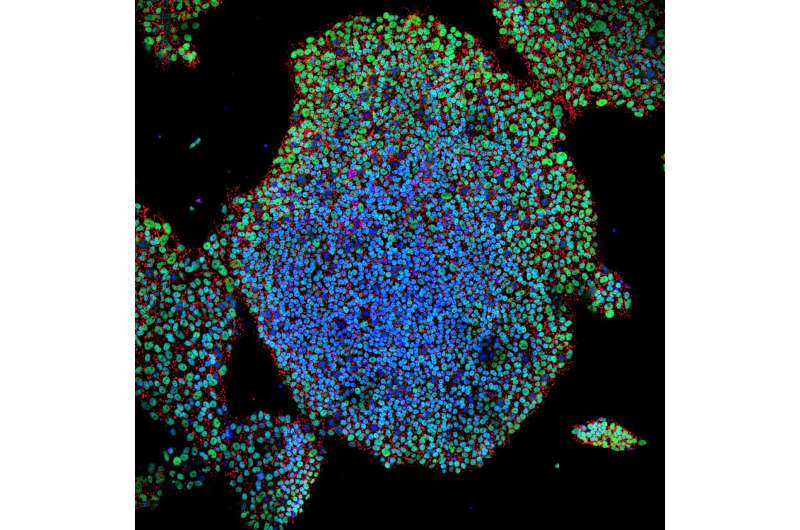
研究人员一直推进从多能干细胞(PSC)产生胰岛素的β细胞,以临床治疗1型糖尿病(T1D)。然而,将这些未成熟细胞移植到患者中造成了大量风险,即肿瘤(Teratomas)的发展和这些干细胞的生长成为不需要的细胞类型。已知多能干细胞发展成所有身体的细胞和组织。
现在,现在,来自迈阿密米勒医学院大学的糖尿病研究所(DRI)的科学家设计了含有两个“自杀基因”的人类多能干细胞系诱导细胞死亡除了所需的胰岛素的生产细胞。这种双重故障安全的方法,在线发布于3月5日问题干细胞报告,解决了psc来源的β细胞的局限性,并为T1D患者创造安全的细胞替代疗法打开了大门。
迫在眉睫的临床试验保证保障
通过使用PSC衍生的β细胞祖细胞已经开始的临床试验和在地平线上具有功能性β样细胞的新方法,需要确保患者安全性至关重要。研究表明,通过当前的PSC分化(显影)方案仅获得约30-40%的β样细胞,留下余额中的显着百分比的未定义细胞。尽管最近的协议改进,但最重要的是,尽管最近的协议改进,但在移植后尚未发展到特定类型的细胞 - 可能会产生肿瘤。
为了解决这些问题,DRI团队开始设计多功能干细胞系,选择性地破坏致瘤细胞和不产生胰岛素的细胞,如肝脏、大脑、肌肉细胞和其他细胞。这个团队测试了他们的方法体外和体内在鼠标模型中糖尿病模仿人类的疾病状况。它们的结果表明除去所有不需要的细胞。
“我们的策略不仅可以防止肿瘤的形成,而且在肿瘤完全发展后,我们才能完全消除它们,”威安Dominguez-Bendala,博士学位,威丹·多明因子 - 博德纳迈阿密米勒医学院糖尿病研究所糖尿病研究所翻译研究与研究副教授的细胞开发。
因此,由于常规的自杀基因的策略引起整个移植物(移植)的破坏或者不选择性地扩增所需细胞的群体,因此没有报告的其他研究方法具有相同程度的安全性和特异性。
虽然该团队专注于衍生胰岛素的细胞,但如果临床成功,这种策略将达到糖尿病的深远。
“通过改变我们自杀盒的一个模块,我们可以使策略成为您选择的任何组织的策略。我们的主要兴趣是β细胞,但也可以根据神经元,心脏或肝细胞选择,例如,“Dominguez-Bendala博士”解释说。
在1型糖尿病中,胰岛素的胰岛素产生的胰岛细胞被免疫系统被错误地破坏,要求患者通过每日胰岛素治疗方案来管理血糖水平。由于DRI科学家发表,胰岛移植患者恢复了1型糖尿病的人们的天然胰岛素生产,但没有足够的细胞来治疗数百万患者可以受益的患者。解决胰岛素的短缺将解决妨碍疾病生物治疗方式的主要挑战之一。
进一步探索











用户评论