2018年8月7日,功能
心脏祖细胞进行细胞命运转向建立冠状动脉
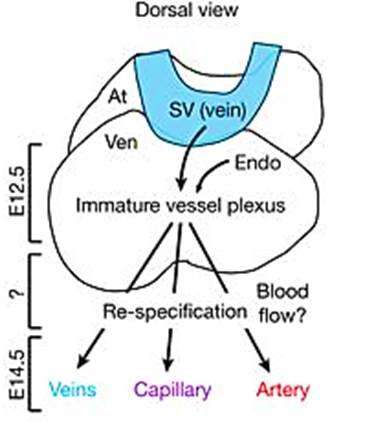
细胞命运和获得新的身份切换器官发生和再生作为一个关键的特征,虽然这类转换机制知之甚少。脉管系统提供了一个生物模型来理解这个过程期间通过区分动脉和静脉胚胎发生通过拮抗转录程序。这些项目包括切口信号保持动脉和COUP-TFs(也称为NR2F2)维持静脉。在胚胎发生过程中,心脏的冠状动脉的一部分来源于静脉称为静脉窦(SV)。静脉可以成为新的动脉的来源在开发期间,尽管vein-to-artery转换的时机和需求是未知的。
一组科学家在心血管医学和生物工程最近开发出一种统计检验分类从单细胞细胞的细胞亚群RNA序列(scRNA-seq)数据集在小鼠遗传学和细胞识别组织指导发展过渡期间心脏的形成。现在发表在自然,工作统计相结合,计算和生物分析的SV冠状动脉转变,显示静脉细胞逐渐从静脉动脉细胞同时交换命运,之前的一个子集细胞交叉转录阈值到pre-artery状态。了解细胞命运开关与抑制性信号在发展将推动现有知识在组织生长和器官形成,改善组织工程策略再生医学。
在这项研究中,Tianying苏等人首次演出一个两步识别和统计分析集群pre-artery内皮细胞亚型,如SV冠状祖细胞(SVc)和SV阀(SVv)使用迭代稳健主成分分析(rPCA),其次是成对不连续性测试。结果证实了模拟和在关系图来识别发展转变内皮的子类型ApjCreER转基因小鼠行。在高分辨率细胞命运的变化进行观察基因表达变化在连续的人口。
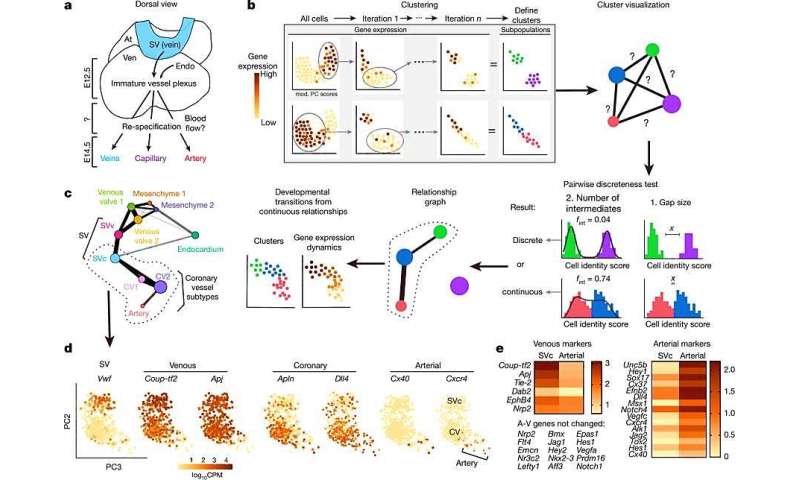
科学家然后删除lineage-labelled内皮细胞从老鼠胚胎的心在一天胚胎12.5 (E12.5)额外的分析。统计协会的解剖关系。值得注意的是,胚胎细胞显示开关对动脉命运生物血流开始前,这些被称为pre-artery细胞。
研究免疫染色也支持胚胎细胞成熟和转换预测。缝隙连接蛋白联接蛋白(CX40),具体到后期胚胎阶段出现在E12.5早些时候,指示pre-artery细胞心脏祖细胞构建的作用大部分成熟的冠状动脉。额外的结构变化后血流在心中形成的起始是归功于剪切应力。
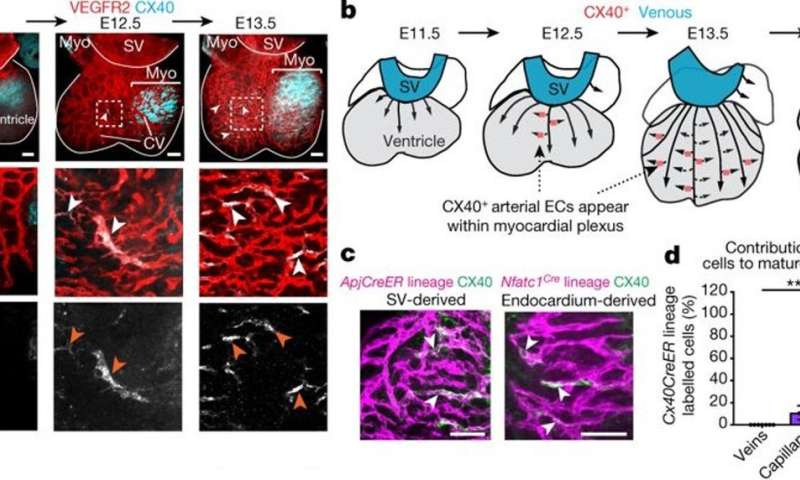
vein-to-artery发展过渡时投射到一个线性连续,单一静脉细胞逐渐减少,细胞的身份走向pre-artery的命运。结果表明,pre-artery规范发生在达到一个阈值的静脉和动脉获得损失;起初,静脉身份的丧失是渐进的,那么动脉身份逐步增加。
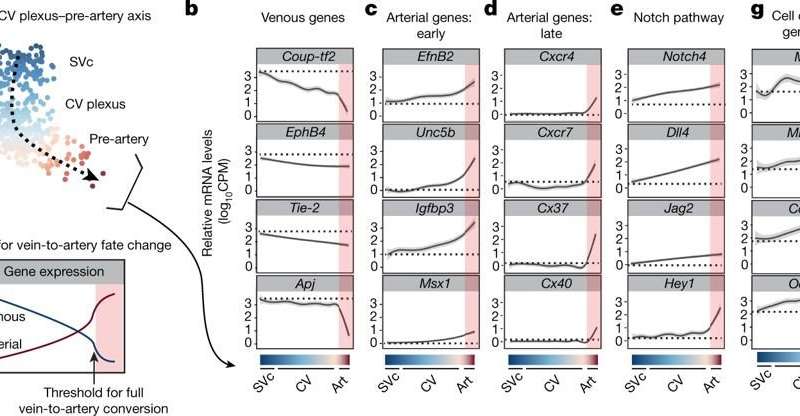
确定这对动脉形成pre-artery规范是必要的,在实验室里研究人员开展了丧失的研究通过阻断这个过程。这是启用COUP-TF2监管机构,通常诱发静脉命运(而得罪动脉的命运)。之前被迫表达COUP-TF2 pre-artery规范阻止细胞造成冠状动脉动脉——建议未能获得pre-artery命运。
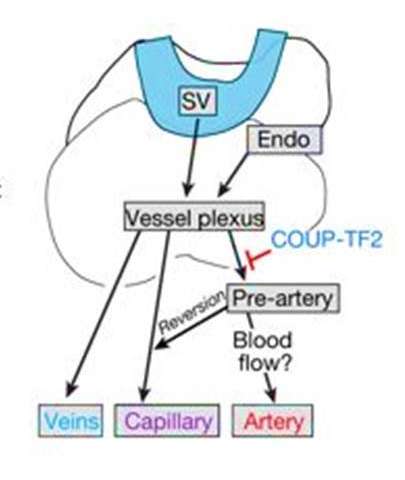
数据显示,开关在命运血管生成逐步发生当个人祖细胞达到一个阈值区分成pre-artery细胞,最终形成成熟的冠状动脉。基础科学研究可以以这种方式提供洞察力来理解细胞机制,提供潜在的治疗应用。未来实验可以在血管生成来帮助调查心脏动脉分化再生疗法的发展。
进一步探索
内皮细胞的祖细胞心脏和血管平滑肌细胞周围的周www.ncbi.nlm.nih.gov pubmed / 27516371陈等人,自然通讯,2016年8月。
面向对象框架健壮的多变量分析www.jstatsoft.org/article/view/v032i03托多罗夫et al,杂志的统计软件,2009年10月。
冠状动脉发展:祖细胞和分化途径www.ncbi.nlm.nih.gov pubmed / 27959616Sharma et al,年度回顾的生理,2017年2月
心内膜细胞形成冠状动脉血管生成通过myocardial-endocardial VEGF信号www.ncbi.nlm.nih.gov pubmed / 23178125吴等人,2012年11月,细胞
基因集富集分析:基于知识的方法解释全基因组表达谱www.ncbi.nlm.nih.gov pubmed / 16199517萨勃拉曼尼亚等,美国国家科学院院刊》上
人类造血干细胞谱系的承诺是一个连续的过程www.ncbi.nlm.nih.gov pubmed / 28319093Velten et al,自然细胞生物学2017年4月,
©2018医疗bob游戏Xpress













用户评论