科学家确定小说的细胞机制,可以导致癌症转移

弗吉尼亚理工大学Carilion研究所的科学家们增加了一个新维度的理解细胞如何改变他们的交流彼此在开发期间,伤口愈合,癌症的扩散。
研究人员在杂志上发表了他们的结果细胞的分子生物学,发表的美国社会细胞生物学》杂志上。
“我们获得了一个新的见解单个细胞如何动态地调节其合成的蛋白质从现有的遗传指令,”詹姆斯·史密斯说,助理教授VTCRI VTCRI心脏和再生医学研究中心和作者的研究。“这微调的理解是新领域。”
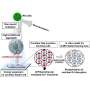
当组织生长或愈合后,其上皮细胞的外层细胞就允许细胞迁移的特性,改变它们的大小和行为,和作为其他细胞类型,特别是多功能间充质细胞是有用的进行维修。这个过程被称为上皮间充质转变,或EMT。
“问题是,EMT也是各种疾病过程中激活,如纤维化和癌症转移,”史密斯说,他也是一个在弗吉尼亚理工大学生物科学学院的助理教授的科学。“幸运的是,这些细胞非常适合操作。我们已经开发了一个强大的新工具来研究这个过程帮助我们得到癌症转移的核心。我们可以观察到癌细胞改变他们的相互交流变得更加侵入性,分离,分散到全身。”
史密斯说,研究人员还可以利用他们的技术来更好地理解细胞反应损伤和疾病在其他疾病,如心脏疾病。
史密斯通常研究心肌细胞之间的沟通,具体关注的角色类型的蛋白质称为联接蛋白43。连接素存在于身体的每一个组织。当六个联接蛋白43蛋白聚集,形成通道缝隙连接通过细胞交流。
历史上,人们认为更多的联接蛋白的蛋白质在细胞中,细胞缝隙连接会越多,从而丰富细胞通讯。
像所有的蛋白质,联接蛋白43从消息编码RNA合成,读出DNA代码。RNA还可以为小块编码或片段的连接素20 k,确保缝隙连接形成。
“这是认为RNA的数量与联接蛋白蛋白质的数量,但我们现在知道它是比这复杂得多,”史密斯说。”的意义蛋白质合成翻译是严格监管的细胞,它是动态的,不断变化的发展和疾病。”
在这项研究中,史密斯发现,RNA和蛋白质合成在EMT联接蛋白增加,但表面的缝隙连接细胞没有增加。
为了理解为什么,史密斯与萨米Lamouille, VTCRI研究助理教授。Lamouille EMT的专家和细胞信号参与蛋白质的翻译,他研究了因为他是旧金山加利福尼亚大学的博士后研究员。
Lamouille,同时也是研究生物科学助理教授在维吉尼亚理工学院的科学,注重理解机制,调节细胞间相互作用在癌症和管制细胞间通信可以通过EMT导致癌症进展。
“在这项研究中,我们发现缝隙连接的结构,使细胞形成的交流中断期间EMT尽管有丰富的联接蛋白43岁“Lamouille说。
正常情况下,细胞使20 k联接蛋白片段全长43联接蛋白直接到计算单元a表面的过程,成为改变缝隙连接形成的损害。
史密斯和Lamouille猜测联接蛋白(20 k)碎片被压制的内部翻译过程中蛋白质合成。
“我们有这种蛋白质的增加,但他们不会细胞膜表面,”史密斯说。“可能连接素被困的地方?”
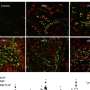
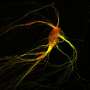
研究人员使用VTCRI的超分辨率显微镜检查单个分子和分析连接素在细胞内。他们发现全身细胞的高尔基体连接素被捕,充当蛋白质包装工厂去细胞的表面。
来抵消的抑制表现20 k联接蛋白片段,史密斯用慢病毒载体导致细胞的RNA 20 k联接蛋白,从而拯救了全身的联接蛋白43岁的缝隙连接的形成,和正常的细胞通讯。
史密斯现在是本研究中他了解到的信息应用到心血管疾病,在那里他看到同样的蜂窝通信问题。
进一步探索