2018年5月23日报告
到底是什么导致了阿尔茨海默氏症,我们又该如何治疗呢?
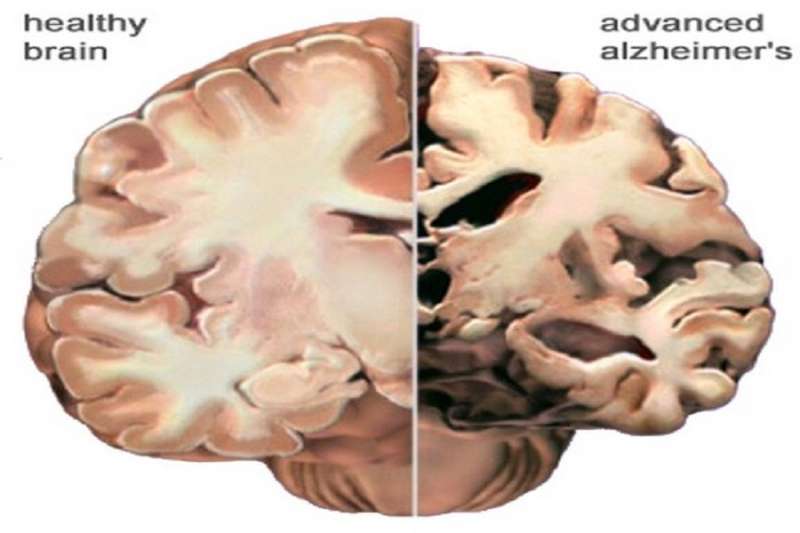
关于阿尔茨海默病的病因有很多理论。他们中的许多人已经产生了这样或那样的实验性治疗。没有一种比从你的香料架上找到任何东西更有效的了。
治疗乙酰胆碱缺乏症的药物,清除淀粉样斑块的疫苗,以及去除过度磷酸化tau的分子伴侣都是未能阻止疾病的潜在疗法。研究人员目前正在研究线粒体功能,以寻找阿尔茨海默症所有病理的可能根源。特别是呼吸复合体的参与电子传递链已经成为一个主要的焦点。
尽管神经斑块和神经纤维缠结等病理与阿尔茨海默氏症相关,但两者都没有被证明是因果关系。证明因果关系的一种方法是用已知的与疾病相关的东西,然后用它来制造疾病。另一种方法是通过控制已知因素来预防疾病。
一篇刚刚发表在bioRxiv上的论文现在表明,研究人员只需要寻找呼吸复合体I的NADH脱氢酶就可以找到可行的靶标。作者能够能够显著延缓老年痴呆症症状的发作动物模型通过RNA干扰(RNAi)敲除复合体I的NDUFA9亚基的表达。通过对2000具尸体大脑的多维人类“组学”数据进行荟萃分析,他们能够确定NDUFA9是阿尔茨海默病的关键元凶。这些数据最近由Sage Bionetworks提供。
他们的动物模型是一种转基因蠕虫,经过工程改造,在其生命周期的特定阶段,在体壁的肌肉细胞中产生类似阿尔茨海默氏症的病理。方便的是,这些变化与容易观察到的蠕虫瘫痪有关。由于这些蠕虫通常以整个细菌为食,因此通过喂食传递RNAi的细菌,可以用RNAi抑制NDUFA9的表达。
研究人员能够证明,RNAi饲料大大降低了整个动物的耗氧量,减少了淀粉样β斑块的毒性,并显著延迟了任何瘫痪。换句话说,就是本垒打。进一步的实验表明,13个额外测试的复合体I亚基中的任何一个的抑制也可以延迟瘫痪。这清楚地确定了NADH脱氢酶是罪魁祸首。
最大的问题是,这一切是如何运作的,因此,我们如何在人类身上实施类似的“治疗”策略?作者认为,温和的复合体I抑制可能对人类具有保护作用。认识到复合体I对人类至关重要是很重要的。当它在基因上被破坏时,就像一些线粒体疾病一样,结果是毁灭性的。在与LHONs综合征和MELAS综合征相关的复合物I亚基中,有几种已知的变异与非常特定和破坏性的病理相关。在利氏综合征中,NDUFA9亚基是许多可以突变的亚基之一。
看来阿尔茨海默病患者可能从一开始就减少了复合物I的表达。这可能反映了身体自然启动的某种代偿机制。像辣椒素或小分子CP2这样的药物可能会进一步抑制复合体i。如果是这样,有一些基准NADH脱氢酶活性的测量来设定适当的剂量将是很重要的。
我们的线粒体与线虫等蠕虫的线粒体有几个主要的区别。我们刚刚报道了琥珀酸脱氢酶(复合物II)如何倒车在一定条件下再生醌电子载体池,用于复合体i。虽然这已被证明发生在几种人类肿瘤的低氧环境中,但尚不清楚这种迷你循环是否对我们也是一件好事。
蠕虫有特殊版本的复杂II子单元,它们可以根据需要交换。他们也有另一种醌电子载体,称为红醌,设计用于特殊复合物II。尽管这些因素在某种程度上使在蠕虫身上的结果外推到人类身上变得复杂,但它们确实为我们提供了对疾病状态下呼吸链活动的更清晰的理解。
更多信息:Safiye Celik等人。利用大数据的概率方法揭示复合物I是阿尔茨海默病的潜在治疗靶点,(2018)。DOI: 10.1101/302737
摘要
通过元分析确定阿尔茨海默病(AD)神经病理学的基因表达标记是一项复杂的工作,因为可用的数据通常来自不同的研究和/或大脑区域,涉及研究特定的混杂因素和/或区域特定的生物学过程。在这里,我们开发了一个基于概率模型的框架DECODER,利用这些差异来识别复杂表型的可靠生物标志物。我们的实验表明:(1)DECODER作为通用元分析框架的潜力,广泛适用于各种疾病(如AD和癌症)和表型(如淀粉样蛋白β;(a β)病理,tau病理和生存),(2)我们从三项研究中使用来自九个大脑区域的1746个人脑组织样本进行荟萃分析的结果——据我们所知,这是对AD最大的表达荟萃分析——以及(3)在表达AD相关a β的转基因秀丽隐杆线虫模型中鉴定的a β毒性修饰物的体内验证,这表明线粒体复合物I是蛋白质平衡的关键中介,是治疗AD的有前途的药理学途径。
©2018 Mbob游戏edical Xpress