实验室培养的人类小脑细胞提供了自闭症的线索
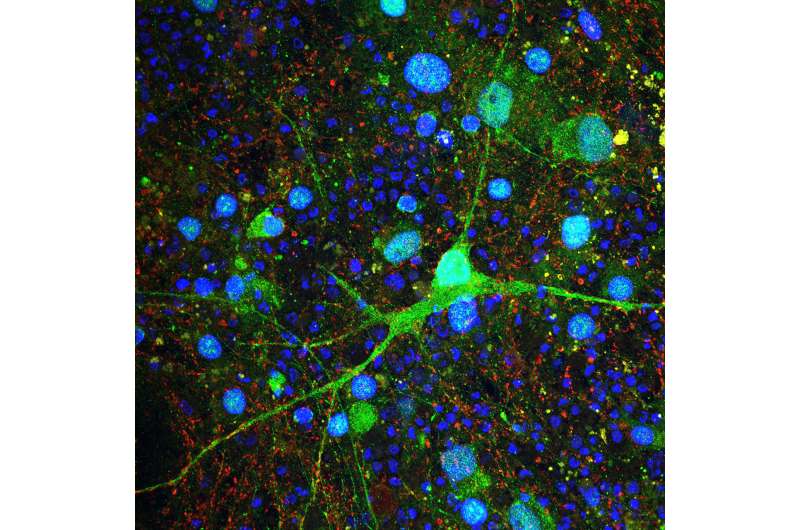
越来越多的证据表明自闭症谱系障碍(ASD)与小脑功能障碍有关,但细节尚不清楚。在一项新的研究中,波士顿儿童医院的研究人员使用干细胞技术,从结节性硬化症(TSC)患者身上培育出了被称为浦肯野细胞的小脑细胞,TSC是一种遗传综合征,通常包括asd样特征。在实验室中,这些细胞显示出一些特征,这些特征可能有助于解释ASD在分子水平上是如何发展的。
由波士顿儿童转化研究中心主任Mustafa Sahin博士领导的研究小组今天在杂志上报告了他们的发现《分子精神病学》.
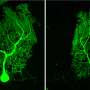
TSC是一种良性肿瘤在身体多个器官中生长的罕见疾病,在大约一半的病例中与ASD有关。先前的大脑解剖表明,TSC患者以及ASD患者的浦肯野细胞数量减少,浦肯野细胞是小脑外交流的主要神经元类型。在2012年的一项小鼠研究中,沙欣和同事敲除浦肯野细胞中的TSC基因(Tsc1),发现小鼠存在社交缺陷和重复行为,同时细胞也出现异常。
在这篇新论文中,沙欣和同事们将他们的观察结果用于人类,研究了来自三名TSC患者的浦肯野病细胞(其中两人也有ASD症状,三人都有癫痫)。
该论文的第一作者Maria Sundberg博士说:“从发育上看,干细胞衍生的神经元接近胎儿状态,概括了细胞的早期分化。”
神经异常
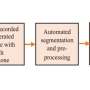
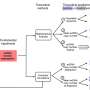
为了制造细胞,桑德伯格首先创造了诱导细胞多能干细胞从病人的血细胞或皮肤细胞,然后将它们微分为神经前体细胞最后是浦肯野细胞。然后,研究小组将它们与来自未受影响的人(父母或性别匹配的对照组)的浦肯野细胞以及使用CRISPR-Cas9基因编辑纠正TSC突变的细胞进行了比较。
“我们看到了变化,”沙欣说。“这些细胞比对照细胞更大,更少放电——这正是我们在小鼠模型中看到的。”
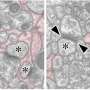
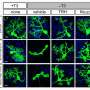
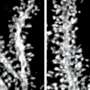
具有TSC遗传缺陷的浦肯野细胞更难与神经祖细胞区分,这表明TSC可能损害小脑组织的早期发育。在检查中,患者来源的浦肯野细胞在树突(神经元用来接收信号的投影)和突触(与其他神经元的连接)发育受损的迹象中显示出结构异常。
TSC浦肯野细胞还表现出一种称为mTOR的细胞生长途径的过度激活。因此,研究小组用雷帕霉素(rapamycin)治疗这些细胞,雷帕霉素是一种mTOR抑制剂,已在临床上用于TSC,以减少TSC相关肿瘤的大小,并预防TSC相关癫痫发作。
将雷帕霉素添加到培养的患者源性细胞中,可以促进更多浦肯野病前体细胞的发育,改善它们突触的功能并增加它们的放电倾向。
最后,研究人员还比较了来自TSC患者和对照组的浦肯野细胞中哪些基因被“打开”。出乎意料的是,患者来源的细胞显示出FMRP的减少,FMRP是一种与脆性X染色体综合征相关的蛋白质,这是ASD和智力残疾的常见遗传原因。已知FMRP有助于调节突触功能,因此它可能有助于在TSC中浦肯野细胞功能异常。
“这些情况可能有一个共同的下游途径,”沙欣说。
分析还显示,突触处两种对神经元间通信很重要的蛋白质的产生减少:突触素和谷氨酸受体蛋白。
一个研究自闭症的平台
该研究首次利用TSC患者自身的干细胞制造出人类浦肯野细胞。在未来的研究中,Sahin和他的同事希望产生更多的患者来源细胞研究单纯TSC患者与同时患有ASD的患者之间的差异。此外,他们希望使用浦肯野细胞平台来研究其他与asd相关的遗传疾病,包括脆性X染色体和SHANK3突变,并测试潜在的药物。桑德伯格还计划为ASD建模创造其他类型的神经元。
“观察特定细胞类型的变化是非常重要的,”Sundberg说。“在TSC中,我们知道在不同的细胞类型中,突变会导致不同的影响。”
进一步探索