细胞质DNA如何引发人类细胞炎症
由LMU的Veit Hornung领导的团队阐明了人类细胞在检测细胞质DNA时诱导炎症的机制。值得注意的是,所涉及的信号网络不同于在相同环境下在小鼠中使用的信号网络。
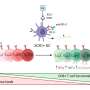
在真核细胞,遗传物质DNA大多局限于细胞核内,而在细胞质中存在细胞核外的DNA则是对细胞有危险的迹象。细胞质DNA可能来自细菌或病毒来源,因此表明感染,或者它可以是内源性来源和精确的组织损伤。因此,先天免疫系统识别其诱导广泛的炎症对策和防御机制。由Veit Hornung教授领导的LMU基因中心的研究人员现在阐明了使先天免疫系统在人体中发挥作用的机制人类细胞来识别这种错位的DNA并触发炎症反应.在这种特殊情况下,Hornung和同事们揭示了人类先天识别过程在进化上基本上是保守的,这一普遍假设是错误的细胞在细胞质DNA识别方面与小鼠细胞有根本不同。新发现发表在最新一期的主要期刊上细胞.
细胞质中游离DNA的存在激活了两种不同的防御措施。第一种是抗病毒免疫反应,由称为干扰素的免疫刺激信使分子的合成和分泌介导。第二种是典型的炎症反应,它会引起发烧和局部肿胀等症状,以使其他免疫细胞招募到紧急部位。一种被称为炎症小体的蛋白质复合物通过激活蛋白质白介素1(炎症的中心介质)在启动炎症级联反应中发挥重要作用。“我们想知道炎症小体是如何识别外源DNA并在人类细胞中引发炎症的,”Hornung说。在之前的研究中,他和他的合作者已经证明了老鼠的细胞,需要一种特殊的dna结合受体来激活炎症小体。
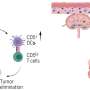
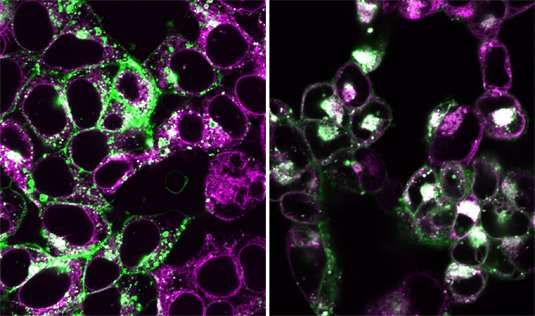
“我们最新的研究表明,在人类骨髓细胞中,这种受体在这一过程中不起作用,因为识别外来或错位DNA的功能模块以不同的方式固定在一起,”Hornung解释道。与小鼠相反,人类骨髓细胞的炎症小体是通过所谓的cGAS-STING识别机制激活的,该机制也负责触发先天免疫反应病毒DNA的存在研究人员现在报告说,cGAS-STING通路的激活导致了独立于抗病毒反应的程序性细胞死亡。“当cGAS-STING通路的激活超过一定阈值时,STING蛋白会诱导一类被称为溶酶体的胞内膜泡的解体,”Hornung团队的博士后、这项新研究的第一作者Moritz Gaidt说。由此产生的细胞损伤然后激活炎症小体,通过分泌白细胞介素1来发出局部紧急状态的信号。Hornung说:“通过这种炎症反应,垂死的细胞警告邻近的细胞,而邻近的细胞反过来又招募免疫细胞到紧急位置。”
这些发现不仅揭示了人类免疫系统的功能,还强调了一个事实,即在模式生物中进行的实验并不总是可靠地转化为人类生物学。Hornung说:“我们的研究以一种典型的方式表明,在人体系统中直接研究这种信号级联是值得的。”
更多信息:莫里茨M.盖特等人。人类髓系细胞中的DNA炎症小体是由NLRP3上游的sting细胞死亡程序启动的,细胞(2017)。DOI: 10.1016 / j.cell.2017.09.039