FUS蛋白病的动态开关
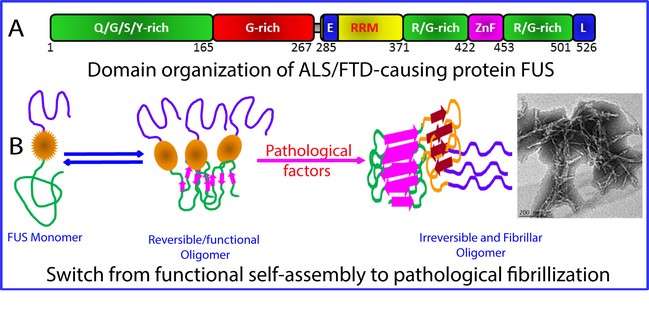
新加坡国立大学生物学家发现,FUS蛋白的动力学在导致某些神经系统疾病的FUS蛋白病中起着关键作用。
肌萎缩性侧索硬化症(ALS)是一种神经系统疾病,会导致控制随意肌肉运动的神经细胞死亡。患有这种疾病的患者随着时间的推移会逐渐变得虚弱,并在日常活动中出现困难,如走路、呼吸和说话。尽管法国神经学家让-马丁·夏科特于1869年首次发现渐冻症,但其发病机制仍然是一个谜,对这种疾病也没有有效的治疗方法。渐冻症是世界范围内常见的神经肌肉疾病。它影响着来自不同种族的人们。这种疾病给病人、他们的家庭和社会带来了巨大的负担。有一项名为“渐冻人症冰桶挑战”的活动来提高人们对这种疾病的认识。
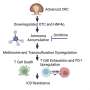
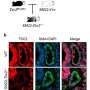
新加坡国立大学生物科学系宋建兴教授领导的团队成功地研究了FUS蛋白及其解剖结构域,这些结构域自然倾向于形成簇。已知FUS蛋白参与ALS和额颞叶痴呆(FTD)的发展。他们的研究表明,FUS的N端和c端低复杂度(LC)结构域本质上是无序的,只有核酸识别结构域(RRM)是折叠的。然而,RRM可以自发地自组装成淀粉样原纤维,它似乎在FUS蛋白病中起着至关重要的作用。宋教授评论说:“研究结果阐明了一个长期存在的难题,即FUS和TDP-43的细胞毒性是由它们结合核酸的能力介导的。”
在过去的几年里,宋教授和他的研究团队一直致力于解码一系列易于聚集的蛋白质的结构、动力学、自组装和膜相互作用。这包括P56S-MSP, SOD1, TDP-43, FUS和大肠杆菌核糖体S1蛋白。他们一直专注于解决一个新出现的极具挑战性的问题,即为什么聚合倾向蛋白可以引发越来越多的人类疾病。他们的研究还涉及到大肠杆菌细胞的老化。这些研究证实,在正常功能和引起神经退行性变的潜力之间存在微妙的平衡,从而支持了神经疾病中的蛋白质聚集可能是聚集蛋白正常功能的夸大这一新兴观点。此外,膜相互作用已被确定为聚合倾向蛋白引发人类疾病和衰老的共同机制。他们对“不溶性”蛋白质的研究支持了这一点,这些研究表明,蛋白质聚集和与膜相互作用的驱动力至少是重叠的,甚至是同一枚硬币的两面。
在未来,研究团队计划更多地关注于理解为什么和如何蛋白质聚合引发细胞老化和人类疾病,超越神经退行性疾病。
林良忠等。als引起的突变显著扰乱TDP-43内在紊乱朊病毒样结构域的自组装和与核酸的相互作用,公共科学图书馆生物学(2016)。DOI: 10.1371 / journal.pbio.1002338
秦海娜等。TDP-43 N端编码了一种新的泛素样折叠及其平衡的展开形式,可以通过与ssDNA结合来改变,美国国家科学院院刊(2014)。DOI: 10.1073 / pnas.1413994112
林建兴歌。用纯水,洞察“不溶性蛋白质”,2月的信(2009)。DOI: 10.1016 / j.febslet.2009.02.022
林建兴歌。通过遗传、病理或环境因素将细胞质蛋白转化为“不溶性”和膜毒性形式,引发疾病/衰老蛋白质和肽信(2017)。DOI: 10.2174 / 0929866524666170209154001