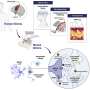
研究目标机制,允许癌症扩散

大多数的女性死于乳腺癌原发恶性肿瘤不会死。他们死侵略性的癌症通过时,迅速蔓延到全身,形成新的骨肿瘤,肺和大脑。
“不幸的是,没有任何治疗地址转移,”塔夫茨大学细胞生物学家迈克尔Forgac说。“这是一个巨大的未满足的临床需要。”
化疗和放疗,典型的癌症治疗,“真的很残酷的技术从生物的角度来看,“Forgac说,教授和发展部门的副主席,在塔夫茨大学医学院分子和化学生物学。虽然这些疗法破坏癌症细胞,他们经常造成间接伤害身体的其他部位,割下来健康的细胞与癌症的。
必须有一个更好的办法,Forgac说,他的工作直接开发目标癌细胞的疗法,让健康组织。一旦研究人员可以解决这个难题,他说,它可能会缩小肿瘤和防止传播没有强有力的影响病人的身体。
萨克勒学校,在他的实验室Forgac专注于小分子结构被称为V-ATPases。他们微型质子泵驻留在一个癌症细胞的外膜和调节pH水平在恶性电路特征,他们的生存是至关重要的。随着病变细胞增长,他说,他们内部产生不寻常的大量的酸。V-ATPases像地下室中的水泵在大雨中,排出多余的酸(而不是水)开始之前杀死细胞。
用药物阻止这些泵工作,Forgac说,研究人员可以陷阱酸在癌症细胞,使细胞更难生存和入侵新tissues-at至少这就是发生在癌细胞在培养皿中培养。
有多大的鱼,但是,当涉及到人类细胞。
癌细胞并不是唯一的依靠V-ATPases-in事实上,几乎每一个细胞都在某种程度上使用我们的身体。在溶酶体,细胞的“胃”V-ATPases发挥重要作用在帮助分解蛋白质的能量。关闭这些细胞泵不加选择地不仅会杀死癌细胞,但也会杀死体内几乎所有其他细胞。
“当我们思考试图癌症治疗的目标(V-ATPases),我们需要找出如何选择性地,“Forgac说。“很明显,如果你在你的身体,抑制所有V-ATPases你死。”
选择一个目标
目标的技巧只是V-ATPases出现在癌细胞在于V-ATPase的结构内一个小细节,Forgac说。
除了一些专门的细胞在体内,V-ATPases大多发现内心深处一个细胞。侵略性的癌症细胞,然而,泵会迁移到细胞的外膜,因为这是一个更好的位置发泄掉多余的酸。所以他们如何到达那里?
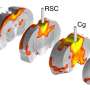
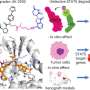
V-ATPase泵放大,你会看到12种不同蛋白质编织成一个复杂的分子机器。他们中的大多数是相同的泵从一个到另一个地方,但在肿瘤细胞,一个特定的部分会在更高的水平。癌细胞的一块更V-ATPase称为a3。Forgac说这件作品作为一种“地址”V-ATPase,指挥它对细胞的表面。
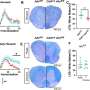
“我们探索V-ATPases数量乳腺癌细胞系,我们发现一般来说,越是浸润性乳腺癌细胞系,a3表达,”他说。如果可以开发药物目标只有V-ATPase水泵有a3块里面,他补充说,有可能在对癌细胞,同时让其他组织完好无损。
说:“这是非常令人兴奋的菲尔•汉德斯教授和系主任的发展,分子和塔夫茨大学化学生物学。“事实上,a3-containing V-ATPases可能候选新药的目标是经过几年的基础研究在迈克尔的一部分。”
这一目标还有很长的路要走,他指出,但一个基本的了解a3是过度,以及它如何指导细胞表面的泵可以创建任何药物之前是至关重要的。
Forgac开始调查a3和癌症之间的联系。而不是孤立地研究癌细胞,他将研究a3如何影响恶性肿瘤在实验室老鼠的传播。
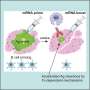
使用DNA编辑技术CRISPR,学生们在他的实验室里将会删除癌细胞的基因负责a3。他们会健康小鼠注入这些编辑癌细胞转移和跟踪他们花多长时间。如果编辑癌症扩散比未经审查的同行更慢,Forgac说,它可能意味着a3确实发挥重要作用在癌症转移到全身。
“这是为下一步,”他说。“如果事实证明我们的假设是真的扰乱或推倒a3减少转移和肿瘤生长便我们可以开始开发工作安全、有效的治疗。”
Forgac的一些工作正在由乳腺癌的100000美元的赠款支持联盟,一个非营利组织在康涅狄格州,基金研究基于疾病。
“我们知道Forgac博士是这个特殊的研究,具有较强的初步数据支持他,”组织的执行主任说,组织者Wattenmaker。
当然,这将是一段时间Forgac的工作导致任何新的乳腺癌治疗。此刻,他主要是做基础研究,探索的方式,实际上这些微小的细胞机制的功能。然而,他感觉强烈,这种基本的了解是任何医学未来发展的基石。
“你不能修复一个破碎的手表,直到你知道手表是如何工作的,”他说。“在医学,这是一样的。理解细胞用于生长和生存的基本过程给你基础开发治疗当这些流程出错。”