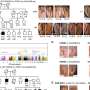
遗传变异决定响应抗糖尿病药物
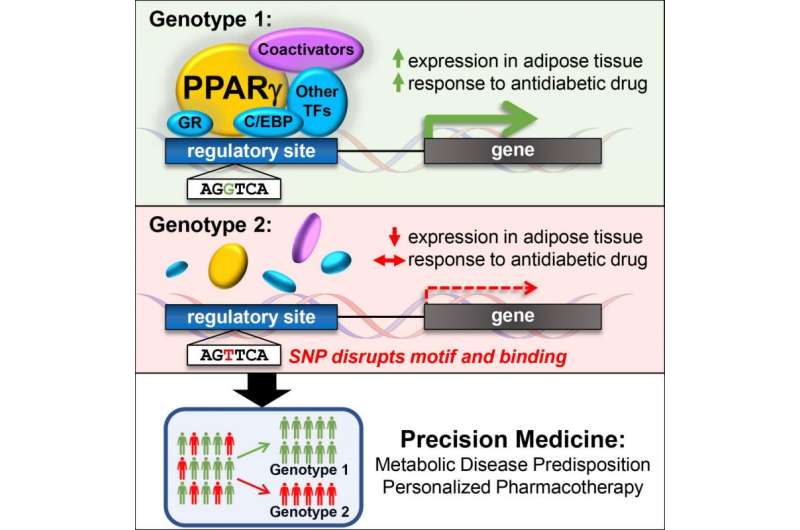
在第一项研究中,宾夕法尼亚大学的研究人员发现一种抗糖尿病药物如何影响变量取决于小自然是个体之间的DNA序列的差异。Raymond Soccio米切尔Lazar,医学博士,医学博士,博士和他的同事们在宾夕法尼亚大学佩雷尔曼医学院的,目的是将这些知识应用到开发个性化的方法治疗糖尿病和其他代谢紊乱。团队在本周公布他们的发现细胞。
Lazar和团队专注于重要的脂肪细胞分子称,γ- ppar的目标thiazolidinedione TZD类药物用于治疗2型糖尿病。在开关与DNA结合,γ- ppar打开其他基因,和宾夕法尼亚大学的研究人员表明,自然遗传差异DNA的监管开关可以确定和TZD药品γ- ppar可以打开其他基因。“这项研究成果的意义超越服用tzd和γ- ppar,所有药物靶点在基因组调节生理功能直接在健康和疾病,“Soccio说,这项研究的首席作者在医学教官。实际上,20%的处方书写是甲状腺激素和类固醇等药物的目标相关的核受体蛋白,γ- ppar Lazar资深作者所指出的,医学和遗传学教授研究所的糖尿病,肥胖和新陈代谢。
被称为单核苷酸多态性的遗传差异,或单核苷酸多态性DNA字母的变体,T、C、G分子自然发生的个体。许多这样的单核苷酸多态性与疾病有关的风险,例如显示,一个人与一个在给定的位置在DNA和别人相比有更高的患糖尿病的危险与g .然而,这些疾病snp经常居住在所谓的“暗物质”并不直接编码基因的基因组,但包括那些开关控制基因。
拉扎尔和他的团队表明,单核苷酸多态性在开关提供一个γ- ppar机制相关联。例如,其中一个SNP与血脂、包括高密度脂蛋白(“好”胆固醇)和甘油三酯;2型糖尿病;高血压;和腰臀比值(“苹果”和“梨”体型肥胖)。这个星座的发现称为“代谢综合征”,和Soccio指出,“值得注意的是,一个改变DNA字母决定是否绑定到一个γ- ppar监管网站在脂肪组织,这可能改变一个人的代谢综合征的风险。”
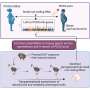
潘队开始动物研究,表明自然单核苷酸多态性之间的不同品系小鼠可以确定其DNA的监管途径γ- ppar开关暗物质的基因组。接下来,他们对待老鼠服用tzd和发现这些单核苷酸多态性也可以确定药物基因。
事实上,一个人的基因构成会影响药物反应导致个性化药物基因组学的相对较新的领域。“我们的研究提供了概念,天然监管遗传变异会影响核受体介导基因活化,更普遍的是,药物反应生活的动物,“Lazar说。“这对服用tzd有着特殊的意义,有强大的抗糖尿病作用但有限的临床效用情况说明,副作用,和不良事件”。
服用tzd是唯一糖尿病药物这一目标脂肪细胞,提高糖尿病患者的胰岛素反应,但他们最近备受争议是因为副作用如水肿和骨质流失,以及报道心脏病和膀胱癌的风险。更重要的是,20%的2型糖尿病患者不能改善他们的糖尿病服用tzd控制。
“总有一天我们在这项研究中使用的方法可以用来预测谁将从TZD-like药物中获益,所以现在我们需要确定的SNP模式差异,可能显示为什么这些药物有好处或伤害一个人,而不是另一个“Soccio解释道。”这种类型的精密医学是研究工作的主要目标。”
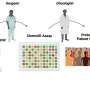
团队开始研究人类脂肪组织,由宾夕法尼亚大学医学肥胖减肥手术病人。类似于老鼠,人类单核苷酸多态性变异也影响绑定γ- ppar DNA调控开关,允许研究人员“审问”这些snp在强大的大型人类遗传研究。他们使用一个芬兰的数据库找到“on”有多少基因在脂肪组织超过1500人表明,单核苷酸多态性影响绑定γ- ppar还确定基因在人类活动水平。最后,他们审问大人类遗传分析称为全基因组关联研究(GWAS),发现单核苷酸多态性影响绑定γ- ppar脂肪构成的一些代谢疾病的风险。
这些研究表明首次绑定γ- ppar自然遗传变异在脂肪细胞DNA可以确定个体疾病风险和药物反应。“我们的工作照强光在约束监管γ- ppar DNA遗传差异,以及这些差异在人们可能会让我们更好地预测代谢性疾病,然后应用精密治疗或预防医学、“Soccio说。