计算机模拟有助于设计具有癌症治疗潜力的分子
通过翻译RNA合成蛋白质依赖于一种叫做eIF4F的蛋白质复合体。由于这种复合物的形成在癌症中通常是不受控制的,因此恢复其调控的能力可能为开发新的癌症疗法铺平道路。由A*STAR p53实验室的Christopher Brown和David Lane以及A*STAR生物信息研究所的Dilraj Lama领导的新加坡团队使用计算机建模设计了可能能够做到这一点的分子。
eIF4F的调控包括破坏复合物中两种蛋白质之间的相互作用,eIF4E和eIF4G。Brown和他的同事们开始用人造肽(或小的蛋白质片段)模拟这种破坏,这些肽以与eIF4G相同的方式与eIF4E结合。为了做到这一点,他们使用一种叫做缩氨酸吻合器的方法来控制缩氨酸结构。
Brown解释说,在整个蛋白质中,多肽通常形成局部结构的部分,但当这些多肽从蛋白质中去除时,它们就变成线性的和高度灵活的。“缩氨酸短钉是一种化学修饰,可以将缩氨酸的两个点连接在一起并重新引入结构。”
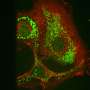
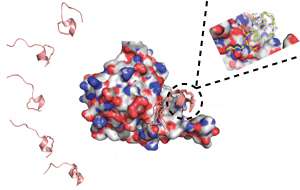
研究小组设计了不同的方案钉肽并通过计算机模拟来揭示它们在与eIF4E结合时和在溶液中自由时的结构。他们还合成了多肽,并通过实验表征了其结构(见图)。
结合实验和模拟获得的信息,显示了改进的潜力。布朗说:“这意味着我们可以设计新的钉住多肽,然后可以通过实验和计算机模拟进一步表征。”“新的设计改变了单个氨基酸。这些改变的目的是优化与eIF4E结合时的肽,或者在溶液中使其看起来更像结合结构。”
利用优化过程,该团队生产了两种与eIF4E强烈相互作用的订钉肽。这需要修改,以便它们的结构在溶液中与与eIF4E结合时保持相同。
布朗说:“我们开发了一种方法来设计与疾病相关的相互作用的高效抑制剂。”“我们的下一步是进一步了解某些固定肽是如何以及为什么具有生物活性,而另一些则没有。”
尽管这些固定肽还没有准备好用于治疗,布朗希望这种情况能很快改变。“在未来,我们设想开发eIF4E订书机肽转化为具有生物活性的分子,并在相关疾病模型中进行测试。”