血红蛋白的研究揭示了我们身体最重要的一分子
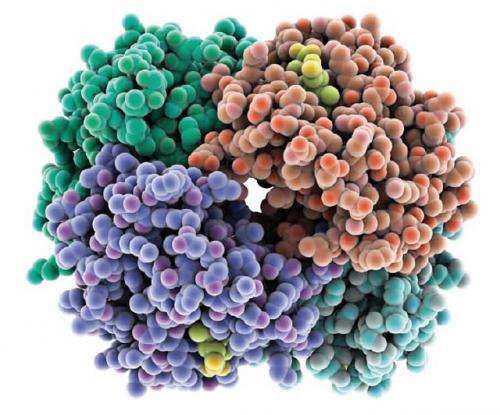
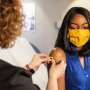
血红蛋白分子存储氧气在体内,和红细胞运输这一至关重要的存储单元在身体周围。血红蛋白的有效运作是至关重要的我们的身体,与血红蛋白不足导致贫血等疾病。因此,重要的是我们理解血红蛋白是如何工作的,什么因素影响其功能。
在这项研究中研究人员观察血红蛋白分子操作优化基于体温通过比较不同动物的血红蛋白的功能。
克里斯·加维和法国和德国的研究人员一直在努力获得更好的理解这个优化涉及的分子基础之间的复杂的相互作用的结构和内部结构的灵活性。
进行这项研究,研究者选择血红蛋白从物种调节身体温度范围的外部条件,包括鸭嘴兽,国内鸡和人类和物种没有调节体温,包括盐水鳄鱼。
研究人员发现,之间存在正相关关系热稳定性这些氧气储存细胞周围的环境(如蛋白质)和它的韧性,阐明血红蛋白是如何进化最好携带氧气在不同身体的温度在不同的物种。
计算机模拟是用来检查哪一部分来自不同物种的血红蛋白分子负责整个柔软的蛋白质的变化。
有了更好的了解血红蛋白的功能,接下来的步骤是检查观察氧亲和力的上下文中,或如何抓住氧血红蛋白分子。这将有可能进一步发展的仪器在ANSTO蛋白石研究反应堆设施。
介绍
分子生物学工具可以在测试假设的功能生物分子通过直接操纵的结构。然而,本研究遵循旧实验的传统,比较生理学,生物方面的功能比较的背景下不同的生理机能。
这种传统方法加上现代软凝聚态科学的工具;计算机模拟与中子和光学光谱,测量动量和能量变化时中子与样品相互作用,揭示蛋白质的柔软的信息。
血红蛋白从物种选择调节体温在一系列外部条件(鸭嘴兽,国内鸡和人类)和一个物种没有调节体温(盐水鳄鱼)。
实验技术显示不仅安排和内部分子的运动变化的基本球状形状也在每一个血红蛋白分子的热稳定性。研究人员发现热稳定性之间的正相关关系这些氧气储存细胞周围的环境(如蛋白质)和它的韧性。
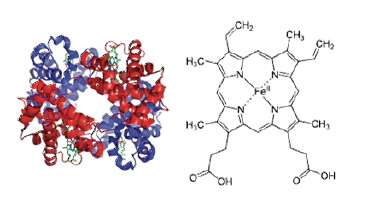
血红蛋白
虽然有高度的相似性血红蛋白分子从不同物种,计算机模拟被用来检查哪一部分来自不同物种的血红蛋白分子负责整个柔软的蛋白质的变化。
有了更好的了解血红蛋白的功能,研究人员正在检查这些观察中氧的亲和力,即如何抓住氧血红蛋白分子,这将有可能进一步发展的仪器在ANSTO蛋白石反应堆设施。
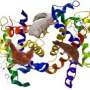
血红蛋白是一种高分子的各种氨基酸(蛋白质),在其原生状态是折叠成一个紧凑的球状形状包括四个独立的血红蛋白分子(图1)。在脊椎动物血红蛋白分子被封闭在一个高度专业化的细胞称为红细胞或血红细胞。Hb4血红蛋白四聚物,主要是发现红细胞内。
的红细胞是最近进化;它存在于大多数脊椎动物的循环,它携带非常浓溶液的氧气储存蛋白质在身体里血红蛋白(大约30%)对代谢过程至关重要。在其正常功能在恒温动物(动物新陈代谢调节体温,如鸭嘴兽、国内鸡和人类)是调节在一个相对狭窄的温度范围,身体的温度。变温动物(如盐水鳄鱼)不新陈代谢调节自己的体温,而是使用行为策略。
生理问题,必须解决的血红蛋白分子是它必须存储从大气中氧气的肺,和小血管的末梢循环中发现许多种类的组织;但它也必须释放氧气,使它可以用于代谢活动。
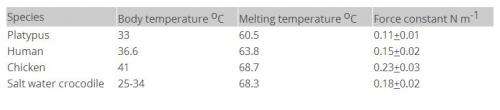
氧气举行的四个血红素组(图1)。各种因素已知影响O2的绑定到这些网站包括其他O2的绑定的四聚物内的其他网站,存在不同的磷酸盐分子与细胞代谢和博士在这项研究中,我们调查了血红蛋白从恒温动物体温和操作的上下文的冷血动物的体温(表1)。
测量
的反向散射光谱仪13[5],[6]领域之中被用来研究的散射中子,中子或改变路径的函数角度以及这些中子的能量变化。获得的信息是氢的平均波动围绕其Hb4分子内的平均位置。氢原子在脊分子这个值很小。
柔和的分子的波动更大,作为温度的函数测量允许我们测量平均力弹性常数。我们的测量表明,一定量的水是必要的获取和维护必要的内部运动血红蛋白的生物功能,也在这个级别的电热力常数的相似之处的体温,也就是说鸭嘴兽有最柔软的血红蛋白和鸡已经笔直的(表1)。
鳄鱼的血红蛋白很严厉对常用其他血红蛋白,但它必须在一系列温度函数。
圆二色性光谱测量光的吸收两种不同极性的差异在紫外/可见政权。这种方法被用来确定不同的折叠的四个血红蛋白分子在整个球状形状作为温度的函数。我们特别关注结构的特定方面的损失,α-helix,使用222 nm的光谱(紫外)地区,和温度有一个部分结构的展开。
我们发现对恒温动物研究的顺序展开的温度是一样的体温。这些测量是用来显示的整体稳定血红蛋白分子的功能结构。

结合计算机模拟的结果
而每个物种的血红蛋白分子很相似,他们都折叠成相同的基本四聚物的球状结构,但是他们巧妙地通过不同的化学链的血红蛋白。我们使用电脑模拟来理解哪些地区的折叠蛋白质负责热稳定性的变化和整体柔软的蛋白质。
第一步是构建一个可靠的三维模型分子的安排在整个球状引导精确的三维结构是未知的鸭嘴兽和鳄鱼血红蛋白。仿真允许我们确定哪些残留负责整个分子的力常数的变化由中子能谱。
的血红蛋白的生物功能分子在不同物种调查周围环境(蛋白质)的刚度氧气储存网站。每个Hb4分子必须函数允许氧气结合,根据生理需要被释放。
我们进一步的调查旨在了解这些观察氧亲和力的环境中,但是我们也推测,一些氧亲和力的介质可能与血红蛋白分子的内部动态的变化。进一步发展仪器的蛋白石反应堆将使我们继续我们的研究在澳大利亚设施。
更多信息:普罗塞,c . l . (1975)。“比较生理学和生物化学的前景。”实验动物学杂志》上194 (1),345 - 347。doi: 10.1002 / jez.1401940122。
Zaccai, g (2000)。“软是一种蛋白质如何?一种蛋白质动态力常数测量中子散射。”[Review].科学288 (5471),1604 - 1607。DOI: 10.1126 / science.288.5471.1604
Benesch, R。,& Benesch, R. E. (1969). "Intracellular Organic Phosphates as Regulators of Oxygen Release By Haemoglobin." [Article].自然618 - 221 (5181),。DOI: 10.1038 / 221618 a0
Stadler a . M。,Garvey, C. J., Bocahut, A., Sacquin-Mora, S., Digel, I., Schneider, G. J., et al. (2012). "Thermal fluctuations of haemoglobin from different species: adaptation to temperature via conformational dynamics."《英国皇家学会界面,2845 - 2855。DOI: 10.1098 / rsif.2012.0364