团队展示了抗生素使肠道致病性感染
一项新的研究由斯坦福大学医学院的研究人员可以帮助确定方法来对抗友好的antibiotics-driven损耗的影响,gut-dwelling细菌。
大量的肠道病原体会导致抗生素管理问题后,贾斯汀松嫩堡说,博士,助理教授微生物学和免疫学和该研究的资深作者,9月1日在网上发表自然。研究生凯瑟琳Ng和杰西卡进球机会共享领导作者。
“这些病原体的抗生素开门。但是,究竟如何发生尚未很好理解,“松嫩堡说。
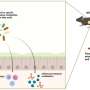
在第一个24小时后管理口服抗生素,一个激增碳水化合物可用性发生在肠道,研究说。这瞬态养分盈余,结合- - -生活友好肠道里的细菌的减少由于抗生素,允许至少有两个潜在的致命的病原体能分到一杯羹,否则更险恶的环境。
在过去的十年左右的时间,有了更多了解微生物生态系统驻留在每一个健康哺乳动物的大肠,包括我们的。成千上万的不同菌株,通常栖息在这挑战但营养丰富的利基已经适应了它,如果没有他们,我们生活有困难了。他们制造维生素,提供关键的培训我们的免疫系统,甚至引导的发展我们自己的组织。抗生素毁掉这gut-microbe生态系统,在几天内开始反弹,但可能需要一个月或者更重拾昔日的数字。和生态系统似乎受到永久的损失部分组成菌株。
人们认为我们的共生体,或友好,细菌作为一种草坪,在征用富人肥料课程通过我们的肠道,战胜less-well-behaved致病“杂草”。It has also been suggested that our commensal bugs secrete pathogen-killing factors. Another theory holds that the disruption of our inner microbial ecosystem somehow impairs our immune responsiveness.
“虽然这些假设绝不是互斥的,我们的工作特别支持建议居民微生物病原体在湾争夺营养,“松嫩堡说。
当防御,是抗生素的课程开始后不久,抢劫微生物如沙门氏菌或艰难梭状芽胞杆菌可以建立滩头阵地。一旦他们达到足够数量,这两个寄生入侵者可以挂载故意运动诱发炎症,是一种损害的恢复正常的肠道生态系统但沙门氏菌和梭状芽孢杆菌学会了繁荣。
特定的营养松嫩堡的团队观察了唾液酸和海藻糖,糖的家人。虽然不是家喻户晓的词汇如葡萄糖、果糖或乳糖,这两种糖品种生产的每一个细胞都在我们的身体,对我们的健康有绝对必要的生存。他们还发现在肉、蛋和奶制品。
细胞肠道挤出长链组成的奇异和熟悉糖联系在一起,被一个统称:粘液。这个简单的产品有两个有价值的功能。首先,通过涂层内部肠壁,粘液形成合理的防渗保护屏障保持居民微生物,胃肠道内有用的用途,从走出肠道进入血液,在那里他们可以是致命的。但粘液第二个函数:它给我们的居民微生物的保证来源各种糖、唾液酸、海藻糖等,他们可以关掉,用在很多方面。例如,他们可以把这些糖分子分解和获得能源。
“我们的肠道微生物已经变得非常擅长吃鼻涕,“松嫩堡说。
为自然研究中,他和他的同事尝试在老鼠身上,生于斯,长于斯在一个无菌的环境。这些老鼠的勇气没有细菌,与正常小鼠港数以百计的细菌种类的肠子和人类一样。这些无菌鼠斯坦福研究者介绍了单一菌株,叫多形拟杆菌。b .θ是一种研究和重要的共生的人类肠道微生物填充。它所必需的酶撬糖分子从肠道粘膜的粘液链流。的唾液酸,它缺乏酶,使其分解这两个分子用于自己的零食。
凿掉糖分子不能肢解食品似乎浪费b .θ的时间。但在一个正常的肠道,还有很多其他微生物消化唾液酸和海藻糖的工具,这可以产生其他材料b .θ的需求。这是一个交换系统,生态学家们称之为共生关系。(也可能是b .θ删削掉这些糖残基到其他食用糖残基下面)。
在一系列独立的实验中,研究人员介绍了美国沙门氏菌感染(沙门氏菌菌株)梭状芽孢杆菌在b .θ)下载实验小鼠。这两种类型的细菌可以引起严重的和潜在的威胁生命的疾病和抗生素的使用有关。他们也有一个共同的能力使用唾液酸作为一种能源,而不是切掉肠道粘液。后发现,梭状芽孢杆菌可以在海藻糖解放和午餐,松嫩堡团队将努力集中在确定两种病原体利用唾液酸。
引入一个友好和一个致病菌株的勇气以前无菌鼠,科学家们能够证明,在这种近似的antibiotic-decimated gut-microbe生态系统,唾液酸的水平飙升至高水平缺乏一套完整的肠道微生物,通常会阻止那些水平攀升。在这些糖的存在和缺乏竞争,病原体都能够复制更快。b .θ生成的唾液酸盈余,在缺乏其他数以百计的正常细菌物种,是留给致病菌株。
当研究人员调查了抗生素对小鼠正常的肠道生态系统的影响,他们看到同样的唾液酸和病原体人口激增的大屠杀。如果老鼠不暴露于病原体,但只有使用抗生素治疗,唾液酸含量恢复到原来的水平大约3天抗生素治疗后同桌的开始恢复。
“坏人清除肠道中营养物质被好人解放,人伤亡的附带损害发生的抗生素,“松嫩堡说。“抗生素导致我们的友好肠道细菌无意中帮助这些病原体。
“我们认为,肠道细菌病原体引起疾病在两个步骤,”他继续说。“他人已经表明,一旦这些病原体达到足够数量,他们使用inflammation-triggering技巧来消灭我们的居民友好的微生物,病原体本身不花钱,因为他们进化的方式来处理它。但首先,他们必须克服的一个关键障碍:缺乏他们试图诱发炎症,他们必须以某种方式达到临界质量。我们的工作显示了他们走后剂量的抗生素。他们利用一个临时激增可用糖从肠道粘液中解放出来杀留下的共生体微生物。"
松嫩堡说,他认为研究人员可能有一天能找到药物,流行性流感减毒活疫苗与抗生素、酶抑制我们的友好肠道菌群可以使用从肠道粘液解放唾液酸,所以不会发生pathogen-nourishing飙升。此外,益生菌的形式菌株特别有才华在消化唾液酸可以达到类似的效果。
进一步探索